题目内容
14.有机物A只含C、H、O三种元素,其相对分子质量为76.为测定A的化学式,取3.8克的A置于密闭容器中完全燃烧,将燃烧产物通过盛有浓硫酸的试剂瓶,试剂瓶增重3.6克,继续通过盛有饱和氢氧化钠溶液的试剂瓶,试剂瓶增重6,6克.(1)A的分子式为C3H8O2;
(2)A只含有一种官能团,且红外光谱图如图1:
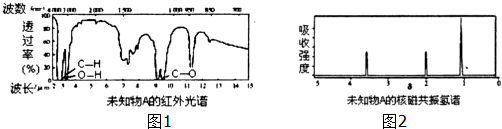
据此推断A可能的结构简式为:(已知:同一个碳原子上连接两个羟基是不稳定的结构)
CH3CH(0H)CH2OH,CH2(OH)CH2CH2OH;
(3)若A的核磁共振氢谱只有三个吸收峰,请写出A与足量金属钠反应的化学方程式:CH2(OH)CH2CH2OH+2Na→NaOCH2CH2CH2ONa+H2↑;
请写出A与氧气(加热,铜做催化剂)反应的化学方程式:CH2(OH)CH2CH2OH+O2$→_{△}^{Cu}$OHCCH2CHO+2H2O.
分析 (1)通过浓硫酸增重3.6g是水的质量,饱和氢氧化钠溶液增重6.6克是生成二氧化碳的质量,根据n=$\frac{m}{M}$计算水、二氧化碳的物质的量,再根据原子守恒计算C原子、氢原子的物质的量,根据m=nM计算C原子、氢原子的质量,进而计算有机物中O原子的质量,根据n=$\frac{m}{M}$计算氧原子的物质的量,确定最简式,结合相对分子质量计算该有机物的分子式.
(2)红外光谱显示A分子中只有“C-C”键、“C-H”键和“O-H”键的振动吸收,据此结合有机物的分子式,推断A可能的结构简式;
(3)A的核磁共振氢谱只有三个吸收峰,分子中含有3种H原子,据此结合A的分子式与红外光谱确定A的结构,书写方程式.
解答 解:(1)通过浓硫酸增重3.6g是水的质量,水的物质的量为:$\frac{3.6g}{18g/mol}$=0.2mol,故n(H)=2×0.2mol=0.4mol,m(H)=0.4mol×1g/mol=0.4g,饱和氢氧化钠溶液增重6.6克是生成二氧化碳的质量,二氧化碳的物质的量为:$\frac{6.6g}{44g/mol}$=0.15mol,故n(C)=0.15mol,m(C)=0.15mol×12g/mol=1.8g,故有机物A中m(O)=3.8g-0.4g-1.8g=1.6g,故n(O)=$\frac{1.6g}{16g/mol}$=0.1mol,所以n(C):n(H):n(O)=0.15mol:0.4mol:0.1mol=3:8:2,最简式为C3H8O2,该最简式中H原子已经达到饱和,则其最简式即为分子式,
故答案为:C3H8O2;
(2)根据图示可知,红外光谱显示A分子中只有“C-C”键、“C-H”键和“O-H”键的振动吸收,同一个碳原子上连接两个羟基不稳定
故符合结构特征的有机物A的结构简式为:CH3CH(0H)CH2OH CH2(OH)CH2CH2OH,
故答案为:CH3CH(0H)CH2OH、CH2(OH)CH2CH2OH;
(3)A的核磁共振氢谱只有三个吸收峰,分子中含有3种H原子,结合有机物A的红外光谱可知,A为CH2(OH)CH2CH2OH,A与足量金属钠反应的化学方程式为:CH2(OH)CH2CH2OH+2Na→NaOCH2CH2CH2ONa+H2↑;
A与氧气(加热,铜做催化剂)反应的化学方程式:CH2(OH)CH2CH2OH+O2$→_{△}^{Cu}$OHCCH2CHO+2H2O,
故答案为:CH2(OH)CH2CH2OH+2Na→NaOCH2CH2CH2ONa+H2↑;CH2(OH)CH2CH2OH+O2$→_{△}^{Cu}$OHCCH2CHO+2H2O.
点评 本题考查有机物分子式、结构简式的确定,题目难度中等,利用原子守恒确定有机物的分子式是解题的关键,注意掌握燃烧法沉淀有机物最简式的原理.

 备战中考寒假系列答案
备战中考寒假系列答案(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ•mol-1):
| 化学键 | C-H | C-F | H-F | F-F |
| 键能 | 414 | 489 | 565 | 158 |
CH4(g)+4F2(g)═CF4(g)+4HF(g)△H=-1928kJ/mol.
(3)下列说法不正确的是(填序号)AD
A.某温度下纯水中的C(H+)=10-6,故其显酸性
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
C.相同温度下,0.1mol•L-1NH4Cl溶液中NH4+的浓度比0.1mol•L-1氨水中NH4+的浓度大;
D.相同温度下,PH均为8的Na2CO3和NaHCO3溶液,前者物质的量浓度大;
E.向饱和石灰水中加入CaO固体,溶液中Ca2+、OH-的物质的量均减小.
| A. | 热稳定性:HCl>H2Se>HBr | B. | 还原性:Se2->S2->Cl- | ||
| C. | 原子半径:Se>Cl>P | D. | 酸性:H2SeO4>H2SO4>H3PO4 |
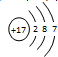 ,C的离子结构示意图
,C的离子结构示意图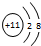 .
. .
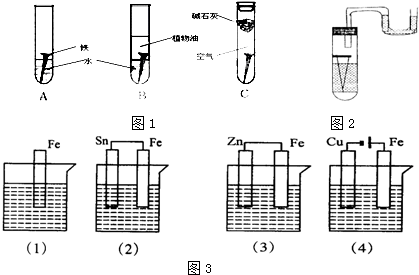
.
 .
.