题目内容
1.对下列有机反应类型的认识中,错误的是( )| A. | 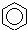 +HNO3$→_{△}^{浓硫酸}$ +HNO3$→_{△}^{浓硫酸}$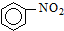 +H2O;取代反应 +H2O;取代反应 | |
| B. | CH4+Cl2→CH3Cl+HCl;置换反应 | |
| C. | CH2=CH2+HCl→CH3-CH2Cl;加成反应 | |
| D. | 2CH3CH2OH+O2$\stackrel{Cu}{→}$2CH3CHO+2H2O;氧化反应 |
分析 有机物中的原子或原子团被其他的原子或原子团所代替生成新的化合物的反应叫取代反应,
断开不饱和双键或三键生成饱和单键的反应属于加成反应,
加氧或去氢的有机反应为氧化反应,据此解答即可.
解答 解:A、苯环上的氢原子被硝基取代生成硝基苯,属于取代反应,故A正确;
B、甲烷中的氢原子被氯原子取代生成CH3Cl,属于取代反应,故B错误;
C、乙烯与氯化氢生成一氯乙烷,不饱和双键变成饱和单键,属于加成反应,故C正确;
D、乙醇与氧气催化氧化生成乙醛属于氧化反应,故D正确,
故选B.
点评 本题考查有机化学反应类型,明确有机物中的官能团及性质的关系,熟悉常见有机物的性质及反应即可解答,题目难度不大.

练习册系列答案
相关题目
11.化学与生活,社会密切相关.下列说法错误的是( )
| A. | 红葡萄酒密封储存时间越长,质量越好,原因之一是贮存过程中生成了有香味的酯 | |
| B. | 透过观察颜色容易区分黄金与铜锌合金 | |
| C. | 乙烯的产量可以用来衡量一个国家的石油化工发展水平 | |
| D. | 燃料电池是一种高效、环境友好的发电装置 |
12.某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹).
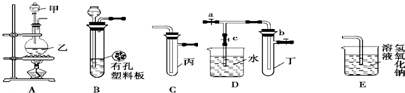
请按要求填空:
(1)利用B装置可制取的气体有H2、CO2(填2种).
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.若在丙中加入适量水,即可制得氯水.将所得氯水分成两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象结论如下:
请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由.实验Ⅰ结论不合理,因为Cl2也有氧化性,此实验无法确定是Cl2还是HClO漂白;实验Ⅱ结论不合理,因为制取的氯气中含有HCl气体,HCl溶于水后能与NaHCO3粉末反应产生气泡
(3)请利用上述A、C装置设计一个简单的实验,验证Cl2和Br2的氧化性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)在甲、乙、丙中分别装入浓盐酸、MnO2、NaBr溶液,烧瓶中有黄绿色气体生成,试管中溶液由无色变为橙色,证明Cl2的氧化性强于Br2.
(4)B、D、E装置相连后,在B中盛装足量浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.B中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹a、b,再打开止水夹c,使烧杯中的水进入试管丁的操作是双手紧握(或微热)试管丁使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流入试管丁.试管丁中的NO2与一定量的O2混合后倒插水中,试管$\frac{9}{10}$充满水,则原试管丁中的混合气体的平均分子量可能为42.08或44.04.(保留二位小数)

请按要求填空:
(1)利用B装置可制取的气体有H2、CO2(填2种).
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.若在丙中加入适量水,即可制得氯水.将所得氯水分成两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象结论如下:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入 NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
(3)请利用上述A、C装置设计一个简单的实验,验证Cl2和Br2的氧化性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)在甲、乙、丙中分别装入浓盐酸、MnO2、NaBr溶液,烧瓶中有黄绿色气体生成,试管中溶液由无色变为橙色,证明Cl2的氧化性强于Br2.
(4)B、D、E装置相连后,在B中盛装足量浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.B中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹a、b,再打开止水夹c,使烧杯中的水进入试管丁的操作是双手紧握(或微热)试管丁使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流入试管丁.试管丁中的NO2与一定量的O2混合后倒插水中,试管$\frac{9}{10}$充满水,则原试管丁中的混合气体的平均分子量可能为42.08或44.04.(保留二位小数)
9. 在常温下A、B、C、D、E是5种常见的气体,F是固体,它们之间存在如下的转化关系,转化关系中涉及的三步反应均是化合反应.已知D分子是含有18个电子的异核双原子分子,E是4核10电子分子.下列说法中不正确的是( )
在常温下A、B、C、D、E是5种常见的气体,F是固体,它们之间存在如下的转化关系,转化关系中涉及的三步反应均是化合反应.已知D分子是含有18个电子的异核双原子分子,E是4核10电子分子.下列说法中不正确的是( )
 在常温下A、B、C、D、E是5种常见的气体,F是固体,它们之间存在如下的转化关系,转化关系中涉及的三步反应均是化合反应.已知D分子是含有18个电子的异核双原子分子,E是4核10电子分子.下列说法中不正确的是( )
在常温下A、B、C、D、E是5种常见的气体,F是固体,它们之间存在如下的转化关系,转化关系中涉及的三步反应均是化合反应.已知D分子是含有18个电子的异核双原子分子,E是4核10电子分子.下列说法中不正确的是( )| A. | 固体F中含有配位键 | B. | D和E分子间均可形成氢键 | ||
| C. | A、B、C三种分子均属于非极性分子 | D. | E分子中中心原子的杂化类型为sp2 |
16.已知某溶液可能含有NH4+、Na+、Mg2+、Al3+、HCO3-、Cl-、NO2-、SO42-中的几种离子.现取3份,此溶液,分别进行如下实验:
①第1份中滴加盐酸,有气体甲产生;
②第2份中滴加用硝酸酸化后的Ba(NO3)2溶液,有白色沉淀产生,过滤后向滤液中加入AgNO3溶液未见沉淀产生;
③第3份中滴加NaOH溶液,先产生白色沉淀,当沉淀增加到一定量后开始产生气体,最后 沉淀完全溶解.
下列判断正确的是( )
①第1份中滴加盐酸,有气体甲产生;
②第2份中滴加用硝酸酸化后的Ba(NO3)2溶液,有白色沉淀产生,过滤后向滤液中加入AgNO3溶液未见沉淀产生;
③第3份中滴加NaOH溶液,先产生白色沉淀,当沉淀增加到一定量后开始产生气体,最后 沉淀完全溶解.
下列判断正确的是( )
| A. | 气体甲可能为纯净物 | |
| B. | 该溶液中一定存在NH4+、Al3+、NO2-、SO42- | |
| C. | 该溶液中一定不存在Na+、Mg2+、HCO3-、Cl- | |
| D. | 无法确定Na+、HCO3-、NO2-是否存在 |
10.化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得到分子式C5H10的两种产物Y、Z,Y、Z经催化加氢后都可得到2-甲基丁烷,若将化合物X用NaOH的水溶液处理,则所得有机产物结构简式可能是( )
| A. | CH3CH2CH2CH2CH2OH | B. | 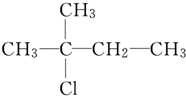 | ||
| C. | 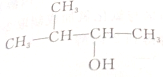 | D. | 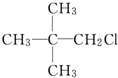 |
17.表1是元素周期表的一部分( 注意:以下各空所涉及的元素填元素符号,不能用字母代替)
(1)C的元素符号为Al;
(2)C的离子的结构示意图 ,
,
(3)用电子式表示AE2的形成过程 G元素的最高价氧化物电子式
G元素的最高价氧化物电子式
(4)H元素的单质的电子式 ;H的氢化物的电子式
;H的氢化物的电子式
(5)A-H八种元素中(填化学式)
(a) 原 子 半径最大的元素是K,原子半径最小的元素是F.
(b)单质的还原性最强的元素是K,单质的氧化性最强的元素是F2
(c)酸性最强的最高价氧化物对应水化物是HClO4;
碱性最强的最高价氧化物对应水化物是KOH.
(6)请设计实验比较B、F的金属性强弱顺序.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O族 |
| 1 | ||||||||
| 2 | G | H | D | |||||
| 3 | B | C | E | |||||
| 4 | F | A | ||||||
(2)C的离子的结构示意图
 ,
,(3)用电子式表示AE2的形成过程
 G元素的最高价氧化物电子式
G元素的最高价氧化物电子式
(4)H元素的单质的电子式
 ;H的氢化物的电子式
;H的氢化物的电子式
(5)A-H八种元素中(填化学式)
(a) 原 子 半径最大的元素是K,原子半径最小的元素是F.
(b)单质的还原性最强的元素是K,单质的氧化性最强的元素是F2
(c)酸性最强的最高价氧化物对应水化物是HClO4;
碱性最强的最高价氧化物对应水化物是KOH.
(6)请设计实验比较B、F的金属性强弱顺序.
| 元素 | 实验设计 | 现象 | 结论 |
| B | 分别在两个盛有滴加酚酞的水的烧杯中加入形状相同的Na和K,观察现象 | K在反应中伴随轻微爆炸,钾比钠的反应更剧烈 | 金属性: K>Na |
| F |