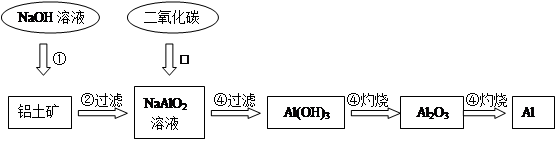
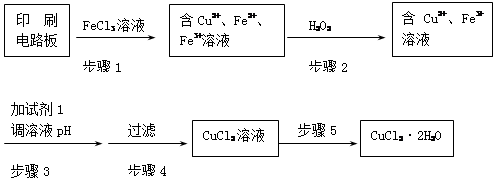题目内容
纯碱、烧碱等是重要的化工原料。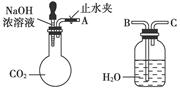
(1)利用上图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是 ,若其他操作不变,将A与C连接,可观察到的现象是 。
(2)向NaOH溶液中通入一定量CO2,结晶后得到白色固体,该白色固体的组成可能是
| A.NaOH和Na2CO3; | |
| B.; | |
| C.; | D.。 |
| 实验操作 | 实验现象 | 结论 |
| (1)取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | | |
| (2) | | |
(1)水沿导管由广口瓶进入烧瓶 广口瓶中的长导管口有气泡产生
(2)Na2CO3 Na2CO3和NaHCO3 NaHCO3
(3)实验操作 实验现象 结论 (1) 产生白色沉淀 CO32? (2)过滤,取少量滤液于试管中,滴加酚酞 滤液变红 有OH-
解析试题分析:(1)把NaOH溶液滴入烧瓶中,CO2与NaOH溶液反应:CO2+2NaOH=Na2CO3+H2O,烧瓶内气体体积减少,压强减小,所以水沿导管由广口瓶进入烧瓶;若其他操作不变,将A与C连接,烧瓶及广口瓶内压强减小,在外界大气压作用下,空气经长导管进入,所以现象为:广口瓶中的长导管口有气泡产生。
(2)CO2可能与NaOH发生反应:CO2+2NaOH=Na2CO3+H2O,CO2+NaOH=NaHCO3,所以白色固体的组成可能是NaOH和Na2CO3;Na2CO3;Na2CO3和NaHCO3;NaHCO3。
(3)要检验A项即NaOH和Na2CO3,加足量BaCl2溶液,若产生白色沉淀,说明含CO32?;加入酸碱指示剂酚酞,可检验OH?。
考点:本题考查实验现象的描述、产物的判断、物质的检验。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案过氧化钠保存不当容易变质,生成Na2CO3。
(1)某过氧化钠样品已经部分变质,请你选择一种溶液 ,证明过氧化钠已经变质。
(2)某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取ag样品,并设计用下图装置来测定过氧化钠的质量分数。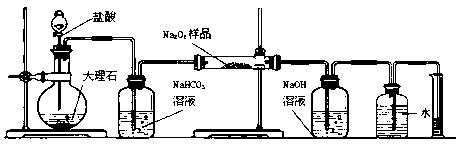
| A. | B. | C. | D.(E)(F) |
①写出装置B中发生反应的离子方程式:
②NaOH的作用是
③他们在读出量筒内水的体积数后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为
某课外小组对一些金属单质和化合物的性质进行研究。
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
| 实验步骤 | 实验现象 |
| ①将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中。 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色。 |
| ②反应结束后分离出溶液备用。 | |
| ③红色固体用蒸馏水洗涤后,置于潮湿空气中。 | 一段时间后固体由红色变为绿色[视其主要成分为Cu2(OH)2CO3]。 |
按实验中发生反应的现象写出下列化学方程式(是离子反应的只写离子方程式)
①析出疏松的红色固体 ;
③一段时间后固体由红色变为绿色 。
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡。持续电解,在阴极附近的溶液中还可观察到的现象是 。
解释此现象的离子方程式是 、 。
(3)工业上可用铝与软锰矿(主要成分为MnO2)反应来治炼金属锰。
①用铝与软锰矿冶炼锰的原理是(用化学方程式表示)
。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是 。
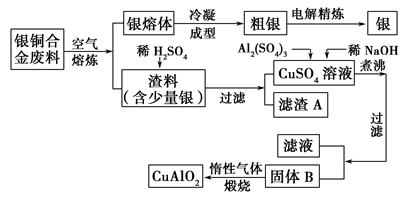
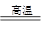 ____CuAlO2+________↑。
____CuAlO2+________↑。
 2Cu + SO2
2Cu + SO2