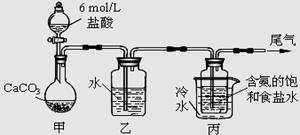
题目内容
过氧化钠保存不当容易变质,生成Na2CO3。
(1)某过氧化钠样品已经部分变质,请你选择一种溶液 ,证明过氧化钠已经变质。
(2)某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取ag样品,并设计用下图装置来测定过氧化钠的质量分数。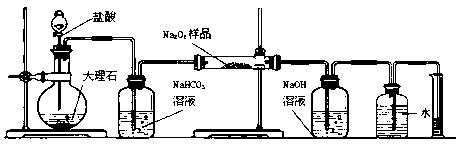
| A. | B. | C. | D.(E)(F) |
①写出装置B中发生反应的离子方程式:
②NaOH的作用是
③他们在读出量筒内水的体积数后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为
(1)BaCl2溶液
(2)①HCO3—+H+ = H2O+CO2↑ ②吸收未反应的CO2 ③
解析试题分析:(1)过氧化钠保存不当容易变质,生成Na2CO3,故检查过氧化钠是否变质,只需检验CO32-,故选用BaCl2溶液。(2)装置B中碳酸氢钠与挥发出来的盐酸反应,离子反应方程式为:①HCO3—+H+ = H2O+CO2↑;②NaOH的作用是吸收未反应的CO2;(3)设样品中过氧化钠的物质的量为:n
2Na2O2 +2H2O═4NaOH+O2↑
2 1
n V×10-3L/22.4L/mol
求得:n= 2V×10-3L/22.4L/mol,故Na2O2的质量为78×2V×10-3L/22.4L/mol,则样品中过氧化钠的质量分数为[(78×2V×10-3g/22.4)/ag] ×100%=
考点:过氧化钠的性质

 阅读快车系列答案
阅读快车系列答案纯碱、烧碱等是重要的化工原料。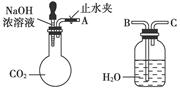
(1)利用上图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是 ,若其他操作不变,将A与C连接,可观察到的现象是 。
(2)向NaOH溶液中通入一定量CO2,结晶后得到白色固体,该白色固体的组成可能是
| A.NaOH和Na2CO3; | |
| B.; | |
| C.; | D.。 |
| 实验操作 | 实验现象 | 结论 |
| (1)取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | | |
| (2) | | |
在实验室里,某同学取一小块金属钠做与水反应的实验。试完成下列问题:
切开的金属钠暴露在空气中,最先观察到的现象是 ,所发生反应的化学方程式是 。
(2)将钠投入水中后,钠融化成一个小球,根据这一现象你能得出的结论是:
① ,② 。
将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是 (填编号)。
| A.有气体生成 | B.钠融化成小球并在液面上游动 |
| C.溶液底部有银白色的金属钙生成 | D.溶液变浑浊 |
(4)根据上述实验过程中钠所发生的有关变化,试说明将金属钠保存在煤油中的目的是 。
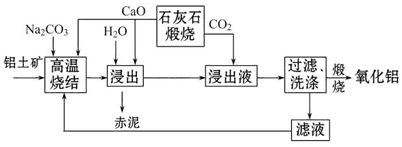






 NaHCO3↓+NH4Cl,处理母液的两种方法:
NaHCO3↓+NH4Cl,处理母液的两种方法: