题目内容
18.已知H3PO4为弱酸,常温下NaH2PO4溶液的pH小于7.下列关于常温下0.10mol•L-1的NaH2PO4溶液的说法正确的是( )| A. | 温度升高,c(H2PO4-)增大 | |
| B. | 加水稀释后,m(H+)与m(OH-)的乘积减少 | |
| C. | c(Na+)+c(H+)=c(OH-)+c(H2PO4-)+2c(HPO42-)+3c(PO43-) | |
| D. | c(Na+)=c(H2PO4-)+c(HPO42-)+C(H3PO4) |
分析 常温下NaH2PO4溶液的pH小于7,说明H2PO4-的水解程度小于其电离程度,
A.升高温度,促进了H2PO4-的电离,溶液中H2PO4-的浓度减小;
B.稀释过程中,H2PO4-的电离程度增大,溶液中氢离子的物质的量增大,但是溶液中氢离子浓度减小,而水的离子积不变,则氢氧根离子浓度增大,氢氧根离子的物质的量、质量增大;
C.溶液中一定满足电荷守恒,根据NaH2PO4溶液中的电荷守恒判断;
D.溶液中一定满足物料守恒,根据NaH2PO4溶液中的物料守恒分析.
解答 解:A.温度升高,H2PO4-的电离程度增大,则溶液中c(H2PO4-)减小,故A错误;
B.加水稀释后,H2PO4-的电离程度增大,溶液中氢离子的物质的量增大,则氢离子的质量增大;由于溶液中氢离子浓度减小,而水的离子积不变,则氢氧根离子浓度增大,氢氧根离子的物质的量、质量增大,故m(H+)与m(OH-)的乘积会增大,故B错误;
C.根据NaH2PO4溶液中的电荷守恒可得:c(Na+)+c(H+)=c(OH-)+c(H2PO4-)+2c(HPO42-)+3c(PO43-),故C正确;
D.根据NaH2PO4溶液中的物料守恒可得:c(Na+)=c(H2PO4-)+c(PO43-)+c(HPO42-)+c(H3PO4),故D错误;
故选C.
点评 本题考查了离子浓度大小比较、弱电解质的电离及其影响,题目难度中等,明确盐的水解、盐的水解原理及其影响为解答关键,注意掌握电荷守恒、物料守恒在判断离子浓度大小中的应用.

练习册系列答案
相关题目
16.下列说法中,正确的是( )
| A. | 分子组成相差一个或几个CH2原子团的物质互为同系物,它们有相似的化学性质和不同的物理性质 | |
| B. | 不带支链的烃,其分子是直线形的 | |
| C. | 甲烷是烷烃中碳含量最低的,也是组成最简单的烃 | |
| D. | 分子式为C4H10的烃有3种 |
6.以CH2=CH2和CH2=CH-CH3混合物为单体,发生加聚反应,可能得到的是( )
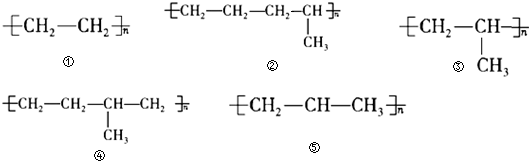

| A. | ①② | B. | ①②⑤ | C. | ①②③⑤ | D. | ①②③④ |
10.饱和食盐水中加入碳酸氢铵可制备小苏打,滤出小苏打后,向母液中通入氨,再冷却、加食盐,过滤,得到氯化铵固体.下列分析错误的是( )
| A. | 该制备小苏打的方程式为:NaCl+NH4HCO3→NaHCO3↓+NH4Cl | |
| B. | 母液中通入的氨气与HCO3-反应:NH3+HCO3-→CO32-+NH4+ | |
| C. | 加食盐是为增大溶液中Cl-的浓度 | |
| D. | 由题可知温度较低时,氯化铵的溶解度比氯化钠的大 |
8.下列说法正确的是( )
| A. | pH=5的NaHSO3溶液中:c(HSO3-)>c(SO32-)>c(H2SO4) | |
| B. | 同浓度的下列溶液中,①NH4HSO4②NH4③NH3•H2O c(NH4+)由小到大的顺序是:②>①>③ | |
| C. | 0.1mol•L-1Na2CO3溶液中:c(HCO3-)=c(H2CO3)+c(H+)-C(OH-) | |
| D. | 0.2mol•L-1CH3COOH溶液和0.2mol•L-1CH3COONa溶液等体积混合:c(CH3COO-)+c(OH-)-c(H+)=0.1mol•L-1 |
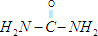 .
. .
.
 .
.