题目内容
15.有机物A与乙酸无论以何种比例混合,只要总质量一定,完全燃烧后产生的水的质量也一定,试回答:(1)若A与乙酸相对分子质量相等,且既能发生银镜反应又能发生酯化反应,则A的结构简式为HOCH2CHO.
(2)若A由四种元素形成的两种官能团组成,相对分子质量与乙酸相等,且分子中氢原子都不与碳原子相连,则A的结构简式为
 .
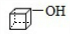
.(3)若A分子中C、H元素质量分数之和为86.67%,其余为O,且A的相对分子质量小于200,则A的分子式为C8H8O.如果A分子中每个碳原子都达到饱和,且能与金属钠反应产生氢气,则A的结构简式为
 .
.
分析 有机物A与乙酸无论以何种比例混合,只要总质量一定,完全燃烧后产生的水的质量也一定,则有机物A中氢元素的质量分数与乙酸中氢元素的质量分数相等为$\frac{1}{15}$.
(1)若A与乙酸相对分子质量相等,既能发生银镜反应又能发生酯化反应,则A含有为-CHO,结合相对分子质量可知,不可能含有-COOH,故A中还有-OH,A与乙酸互为同分异构体;
(2)若A的相对分子质量与乙酸相等,则A的分子量为60,分子中H原子数目为4,由碳、氢、氧、氮四种元素组成,则1个C原子、O原子、N原子与4个H原子的相对原子质量之和=12+16+14+4=46,相对分子质量还差60-46=14,为1个N原子,所以分子式为CH4ON,分子中含有两种官能团,且分子中氢原子都不与碳原子相连,则分子中含有-NH2与羰基;
(3)根据氧元素的质量分数计算氧原子最大数目,确定含有O原子数目,进而计算有机物的相对分子质量,再计算分子中H原子数目,进而计算C原子数数目,确定分子式,再根据能与钠反应生成氢气,确定含有的官能团,结合有机物的结构特点确定其结构.
解答 解:有机物A与乙酸无论以何种比例混合,只要总质量一定,完全燃烧后产生的水的质量也一定,则有机物A中氢元素的质量分数与乙酸中氢元素的质量分数相等为$\frac{1}{15}$.
(1)若A与乙酸相对分子质量相等,既能发生银镜反应又能发生酯化反应,则A含有为-CHO,结合相对分子质量可知,不可能含有-COOH,故A中还有-OH,A与乙酸互为同分异构体,A与乙酸互为同分异构体,分子式为C2H4O2,所以符合条件的结构简式为:HOCH2CHO,
故答案为:HOCH2CHO;
(3)若A的相对分子质量与乙酸相等,则A的分子量为60,分子中H原子数目为4,由碳、氢、氧、氮四种元素组成,则1个C原子、O原子、N原子的相对原子质量之和加4个H原子相对原子质量=12+16+14+4=46,相对分子质量还差60-46=14,为1个N原子,所以分子式为CH4ON2,分子中含有两种官能团,且分子中氢原子都不与碳原子相连,则分子中含有-NH2与羰基,所以符合条件的结构简式为“ ,
,
故答案为: ;
;
(3)若A分子中C、H元素质量分数之和为86.67%,其余为O,且A的相对分子质量小于200,则分子中氧原子最大数目=$\frac{200×(1-86.67%)}{16}$=1.6,故分子中含有1个O原子,故该有机物的相对分子质量=$\frac{16}{1-86.67%}$=120,故分子中N(H)=$\frac{120×\frac{1}{15}}{1}$=8,故N(C)=$\frac{120-16-8}{12}$=8,故该有机物分子式为C8H8O,A能与金属钠反应产生氢气,含有-OH,A分子每个碳原子都达到饱和,含有环状,则A的结构简式为 ,
,
故答案为:C8H8O; .
.
点评 本题考查有机物结构式的确定,难度中等,判断有机物A中氢元素的质量分数与乙酸中氢元素的质量分数相等是关键.

| A. | Na+、Ca2+、Cl-、HCO3- | B. | Mg2+、Na+、SO42-、Cl- | ||
| C. | K+、Na+、NO3-、MnO4- | D. | NH4+、Al3+、NO3-、OH- |
| A. | 稀盐酸 | B. | 氢氧化钠溶液 | C. | FeCl3溶液 | D. | 高锰酸钾溶液 |
| A. | 18O、19O、24Mg | B. | 12C、31P、27Al | C. | 第ⅤA族原子 | D. | 第三周期原子 |
| A. | A3BC4 | B. | A2(BC4)3 | C. | A2BC3 | D. | A2BC4 |
| A. | 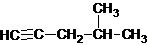 2-甲基-4-戊炔 2-甲基-4-戊炔 | |
| B. | CH2=C(C2H5)22-乙基-1-丁烯 | |
| C. | CH3CH(CH3)CH2CH(C2H5)CH3 2-甲基-4-乙基戊烷 | |
| D. | 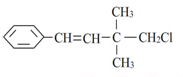 1,3,5-三硝基甲苯 1,3,5-三硝基甲苯 |
| A. | 温度升高,c(H2PO4-)增大 | |
| B. | 加水稀释后,m(H+)与m(OH-)的乘积减少 | |
| C. | c(Na+)+c(H+)=c(OH-)+c(H2PO4-)+2c(HPO42-)+3c(PO43-) | |
| D. | c(Na+)=c(H2PO4-)+c(HPO42-)+C(H3PO4) |
 ;D、E的最高价氧化物对应水化物发生反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O; A、C形成的化合物中,C的质量分数最高的化合物的结构式H-O-O-H;A有多种同位素,其中一种同位素原子核内有两个中子,这种同位素原子的符号是31H或T.
;D、E的最高价氧化物对应水化物发生反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O; A、C形成的化合物中,C的质量分数最高的化合物的结构式H-O-O-H;A有多种同位素,其中一种同位素原子核内有两个中子,这种同位素原子的符号是31H或T. 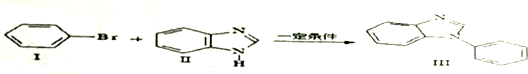
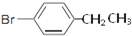 、
、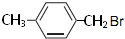 .
.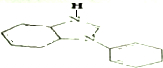 .
.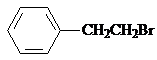 ,Ⅴ与氢氧化钠醇溶液加热条件下反应的方程式为:
,Ⅴ与氢氧化钠醇溶液加热条件下反应的方程式为: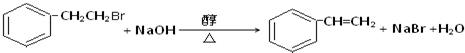 .
.