题目内容
13.在一定温度下的在2L密闭容器中加入一定量的炭和水蒸气发生如下反应:C(s)+H2O(g)?CO(g)+H2(g)△H>0,可认定该可逆反应在一定条件下已达到化学平衡状态的是( )| A. | 容器中H2O、CO、H2的物质的量之比为1:1:1 | |
| B. | v正(CO)=v逆(H2O) | |
| C. | 生成n molCO的同时生成n mol H2 | |
| D. | 1mol H-H键断裂同时生成2mol H-O键 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、当体系达平衡状态时,容器中H2O、CO、H2的物质的量之比可能为1:1:1,也可能不是,与各物质的初始浓度及转化率有关,故A错误;
B、v正(CO)=v正(H2O)=v逆(H2O),故B正确;
C、都体现的正反应方向未体现正与逆的关系,故C错误;
D、都体现的是逆向,未体现正与逆的关系,故D错误;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
4.由一个O,一个N,7个H和若干个碳原子组成的有机物,其碳原子的个数至少为( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
1.如图为铜锌原电池示意图,下列说法正确的是( )
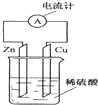

| A. | 电子由铜片通过导线流向锌片 | B. | 锌片逐渐溶解 | ||
| C. | 烧杯中溶液逐渐呈蓝色 | D. | 该装置能将电能转变为化学能 |
8.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=13的溶液:K+、Na+、Cl-、SiO32- | |
| B. | c(H+)/c(OH-)=1×10-14的溶液:Na+、NH4+、Cl-、SO42- | |
| C. | 0.1mol•L-1的Na2CO3溶液:Na+、Ca2+、I-、SO42- | |
| D. | 加入石蕊呈蓝色的溶液:Na+、Al3+、Cl-、NO3- |
5.a g CO 和H2的混合气体在足量O2中完全燃烧后,将产生的CO2和水蒸气通入过量的过氧化钠被其完全吸收,问过氧化钠固体质量增加多少g.( )
| A. | a g | B. | 0.5a g | C. | 4.4a g | D. | 1.8a g |
2.下列反应的离子方程式书写正确的是( )
| A. | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++H2O | |
| B. | 澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- |
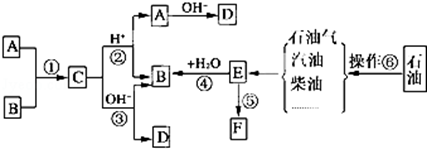
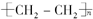 .
. ,写出M在催化剂作用下缩聚为高分子化合物的反应方程式
,写出M在催化剂作用下缩聚为高分子化合物的反应方程式 +(n-1)H2O.另有有机物N在浓硫酸存在下,两分子相互作用生成一种环状酯
+(n-1)H2O.另有有机物N在浓硫酸存在下,两分子相互作用生成一种环状酯 ,则有机物N的结构简式为:
,则有机物N的结构简式为: .M溶液既能和Na反应,又能和NaOH溶液反应,写出M与Na反应的反应方程式:
.M溶液既能和Na反应,又能和NaOH溶液反应,写出M与Na反应的反应方程式: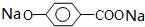 +H2↑.
+H2↑.