题目内容
【题目】请回答下列问题.
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度. 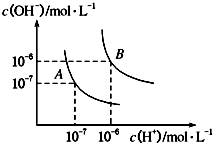
①100℃时1molL﹣1的NaOH溶液中,由水电离出的c(H+)=molL﹣1 , KW(25℃)KW(100℃)(填“>”、“<”或“=”).
②25℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是(填“促进”、“抑制”或“不影响”).
(2)电离平衡常数是衡量弱电解质电离程度强弱的量.已知如表数据.
化学式 | 电离平衡常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
①25℃时,有等浓度的a.NaCN溶液 b.CH3COONa 溶液 c.Na2CO3溶液,三种溶液的pH由大到小的顺序为;(填序号)
②25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,则c(Na+)c(CH3COO﹣)(填“>”、“<”或“=”).
【答案】
(1)1×10﹣12;<;促进
(2)c>a>b;>
【解析】解:(1)①水的电离时吸热过程,加热促进电离氢离子浓度和氢氧根离子浓度增大,Kw增大,所以Kw(25℃)<Kw(100℃); A点c(H+)=c(OH﹣)=10﹣7 mol/L,Kw=c(H+)c(OH﹣)=10﹣14 , 故A点为25℃;B点c(H+)=c(OH﹣)=10﹣6 mol/L,Kw=c(H+)c(OH﹣)=10﹣12 , 故B点为100℃.
100℃时1molL﹣1 的NaOH溶液中Kw=c(H+)c(OH﹣)=10﹣12 ;c(OH﹣)=1mol/L,水电离出的c(H+)=1×10﹣12;
所以答案是:1×10﹣12 , <;
②NH4Cl固体溶解后溶液中铵根离子水解生成一水合氨和氢离子,溶液呈酸性,水的电离被促进;
所以答案是:促进;(2)①根据图表数据分析,电离常数:醋酸>HCN>碳酸氢根离子,所以等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度为:Na2CO3溶液>NaCN溶液>CH3COONa溶液,故溶液的pH为:c>a>b;所以答案是:c>a>b;
②25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,恰好完全反应生成醋酸钠,而醋酸钠是强碱弱酸盐,弱酸根离子水解,所以c(Na+)>c(CH3COO﹣),所以答案是:>.
【考点精析】根据题目的已知条件,利用弱电解质在水溶液中的电离平衡的相关知识可以得到问题的答案,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.