题目内容
一定条件下,可逆反应:X(g) + 3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),反应达到平衡时, X、Y、Z的浓度分别为0.1mol?L-1、0.3 mol?L-1、0.08 mol?L-1,则下列判断不正确的是 ( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),反应达到平衡时, X、Y、Z的浓度分别为0.1mol?L-1、0.3 mol?L-1、0.08 mol?L-1,则下列判断不正确的是 ( )
| A.c1∶c2="=" 1∶3 | B.平衡时,Y和Z生成速率之比为3∶2 |
| C.X、Y的转化率不相等 | D.c1的取值范围为0< c1< 0.14 mol?L-1 |
C
解析试题分析:A.因为X、Y发生反应时的物质的量的比是1:3,平衡时二者的物质的量的比也是1:3,说明开始浓度的比为1:3,正确;B.在方程式中Y、Z的系数比是3:2,一种是反应物,一种是生成物,若平衡时,Y和Z生成速率之比为3∶2,则二者的浓度都不变,反应达到平衡,正确;C.由于X、Y的系数关系、开始投入都是1;3,所以它们的转化率是相等的,错误;D.若反应是从正反应方向开始的,则c1的值是,4mol/L;若反应是从逆反应方向开始的,则c1的值是0,由于X、Y、Z的起始浓度分别为c1、c2、c3(均不为零)因此c1取值范围为0< c1< 0.14 mol?L-1,正确。
考点:考查可逆反应的物质浓度、化学反应速率、物质的转化率及浓度的取值范围的知识。

 阅读快车系列答案
阅读快车系列答案常温下钛的化学活性很小,在较高温度下可与多种物质反应。
(1)工业上由金红石(含TiO2大于96%)为原料生产钛的流程如下: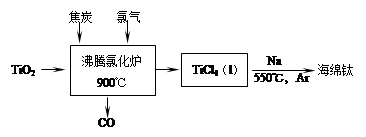
① 沸腾氯化炉中发生的主要反应为: 。
②已知:Ti(s) +2Cl2(g)=TiCl4(l) ΔH=a kJ·mol-1;
2Na(s) +Cl2(g)=2NaCl(s) ΔH=b kJ·mol-1;
Na(s)=Na(l) ΔH=c kJ·mol-1;
则TiCl4(l) +4Na(l)=Ti(s) +4NaCl(s) ΔH= kJ·mol-1。
③ TiCl4遇水强烈水解,写出其水解的化学方程式 。
(2)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氯化钙,原理如图所示,二氧化钛电极连接电 极,该极电极反应为: 。但此法会产生有毒气体,为减少对环境的污染,在电池中加入固体氧离子隔膜(氧离子能顺利通过),将两极产物隔开,再将石墨改为金属陶瓷电极,并通入一种还原性气体,该气体是 。
(3)海绵钛可用碘提纯,原理为: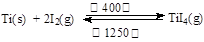 ,下列说法正确的是 。
,下列说法正确的是 。
| A.该反应正反应的ΔH>0 |
| B.在不同温度区域,TiI4的量保持不变 |
| C.在提纯过程中,I2 的作用是将粗钛从低温区转移到高温区 |
| D.在提纯过程中,I2 可循环利用 |
在一定温度下,容器内某一反应中两种气态物质M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
A.反应的化学方程式为:2M N N |
| B.t2时,正逆反应速率相等,反应达到平衡状态 |
| C.t3时,M上a点正反应速率等于N上b点的逆反应速率 |
D.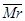 混一定时,N的体积百分含量也一定 混一定时,N的体积百分含量也一定 |
在密闭容器中进行反应:X(g)+3Y(g) 2Z(g),有关下列图像的说法正确的是
2Z(g),有关下列图像的说法正确的是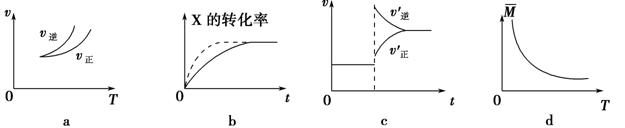
| A.依据图a可判断正反应为吸热反应 |
| B.在图b中,虚线可表示压强增大 |
| C.若正反应的ΔH<0,图c可表示升高温度使平衡向逆反应方向移动 |
| D.由图d中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0 |
在一定温度下的恒容密闭容器中,能说明反应X2(g)+ Y2(g) 2XY(g) 已达到平衡的是( )
2XY(g) 已达到平衡的是( )
| A.容器中的总压不随时间变化 |
| B.容器中的气体平均相对分子质量不随时间变化 |
| C.容器中的混合气体的密度不随时间变化 |
| D.容器中的各种气体的质量分数不随时间变化 |
对于反应 A + B 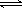 C,下列条件的改变一定能使化学反应加快的是
C,下列条件的改变一定能使化学反应加快的是
| A.升高体系的温度 | B.增加A的物质的量 |
| C.减少C的物质的量 | D.增大体系的压强 |
已知2SO2 (g)+O2 (g)  2SO3 (g);△H =﹣197kJ?mol﹣1,向同温、同体积的三个密闭容器中分别充入气体,起始投料量如下表:
2SO3 (g);△H =﹣197kJ?mol﹣1,向同温、同体积的三个密闭容器中分别充入气体,起始投料量如下表:
| | SO2 (mol) | O2 (mol) | SO3 (mol) |
| 甲 | 2 | 1 | 0 |
| 乙 | 4 | 2 | 0 |
| 丙 | 0 | 0 | 2 |
恒温、恒容下反应达平衡时,下列关系一定正确的是
A.SO3的质量m:2m甲 = m乙
B.容器内压强P:2P丙 > P乙
C.反应放出或吸收热量的数值Q:Q甲 > Q丙
D.c(SO2)与c(O2)之比a:a丙 > a乙
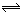 H2(气)+I2(气)已达平衡状态的是
H2(气)+I2(气)已达平衡状态的是 2NH3(g) △H="—92.4" KJ/mol。在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1 mol NH3。现在相同条件下的同一容器中充入x mol N2,y mol H2和2 mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2KJ。则x、y的值分别为( )
2NH3(g) △H="—92.4" KJ/mol。在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1 mol NH3。现在相同条件下的同一容器中充入x mol N2,y mol H2和2 mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2KJ。则x、y的值分别为( )