题目内容
已知N2(g)+3H2(g) 2NH3(g) △H="—92.4" KJ/mol。在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1 mol NH3。现在相同条件下的同一容器中充入x mol N2,y mol H2和2 mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2KJ。则x、y的值分别为( )
2NH3(g) △H="—92.4" KJ/mol。在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1 mol NH3。现在相同条件下的同一容器中充入x mol N2,y mol H2和2 mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2KJ。则x、y的值分别为( )
| A.1.5, 6.5 | B.2, 8 | C.5, 21 | D.3, 13 |
C
解析试题分析: N2(g)+3H2(g) 2NH3(g)
2NH3(g)
开始 2 8 0
转化 0.5 1.5 1
平衡 1.5 6.5 1
氮气的转化率为0.5mol/2mol=25%,放出热量为46.2kJ;
相同条件下的同一容器中充入xmol N2,ymol H2和2mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2kJ,则二者为等效平衡,所以
N2(g)+3H2(g) 2NH3(g)
2NH3(g)
开始 x y 2
等效 x+1 y+3
则:(x+1)/(y+3)=2mol/8mol=1/4,
解得4x+1=y,
A.4×1.5+1≠6.5,故A错误;
B.4×2+1≠8,故B错误;
C.5×4+1=21,由放出的热量设氮气转化nmol,则92.4n-92.4=46.2,所以n=1.5mol,氮气的转化率为25%,故C正确;
D.3×4+1=13,由放出的热量设氮气转化nmol,则92.4n-92.4=46.2,所以n=1.5mol,氮气的转化率为37.5%,故D错误;
故选C。
考点:化学平衡的计算。

一定条件下,可逆反应:X(g) + 3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),反应达到平衡时, X、Y、Z的浓度分别为0.1mol?L-1、0.3 mol?L-1、0.08 mol?L-1,则下列判断不正确的是 ( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),反应达到平衡时, X、Y、Z的浓度分别为0.1mol?L-1、0.3 mol?L-1、0.08 mol?L-1,则下列判断不正确的是 ( )
| A.c1∶c2="=" 1∶3 | B.平衡时,Y和Z生成速率之比为3∶2 |
| C.X、Y的转化率不相等 | D.c1的取值范围为0< c1< 0.14 mol?L-1 |
用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,当反应达到平衡时,下列说法正确的是( )
| A.18O只存在于乙酸乙酯中 | B.18O存在于水、乙酸、乙醇以及乙酸乙酯中 |
| C.18O存在于乙酸乙酯、乙醇中 | D.若与丙酸反应生成酯的相对分子质量为102 |
定容容器中反应:N2(g)+3H2(g) 2NH3(g),下列措施不能提高其反应速率的是( )。
2NH3(g),下列措施不能提高其反应速率的是( )。
| A.升高温度 | B.使用催化剂 |
| C.充入稀有气体,增大体系压强 | D.增加N2和H2的起始量 |
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
下列描述正确的是
| A.反应开始到10s,用Z表示的反应速率为0.158 mol·L-1·s-1 |
| B.反应开始到10s,X的物质的量浓度减少了0.79 mol·L-1 |
| C.反应开始到10s,Y的转化率为79.0% |
D.反应的化学方程式为:X(g) + Y(g) Z(g) Z(g) |
对于100mL 1mol/L盐酸与锌粒的反应,采取下列措施能使反应速率加快的是①升高温度;②改用100mL 3mol/L盐酸;③改用300mL 1mol/L盐酸;④用等量锌粉代替锌粒;⑤滴入少量CuSO4溶液
| A.①②④⑤ | B.①③④⑤ | C.①②③④ | D.①②④ |
在容积一定的密闭容器中,反应2A B(g)+C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是 ( )
B(g)+C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是 ( )
| A.正反应是放热反应,且A是气态 |
| B.正反应是吸热反应,且A不是气态 |
| C.其他条件不变,加入少量A,该平衡向正反应方向移动 |
| D.改变压强对该平衡的移动无影响 |
 2Q(g)
2Q(g)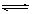 2C(g)(正反应吸热),下列图象中正确的是
2C(g)(正反应吸热),下列图象中正确的是