题目内容
下列方法中可以证明2HI(气) H2(气)+I2(气)已达平衡状态的是
H2(气)+I2(气)已达平衡状态的是
① 单位时间内生成n mol H2的同时生成n mol HI
② 一个H-H键断裂的同时有两个H-I键断裂
③温度和压强一定时混合气体密度不再变化
④ 反应速率υ(H2)=υ(I2)=0.5υ(HI)时
⑤ c(HI)=c(H2)=c(I2)=2:1:1
⑥ 温度和体积一定时,某一生成物浓度不再变化
⑦ 温度和体积一定时,容器内压强不再变化
⑧ 条件一定,混合气体的平均相对分子质量不再变化
⑨ 温度和体积一定时混合气体的颜色不再变化
| A.②③④⑤⑥ | B.②⑥⑦⑧⑨ | C.①②⑥⑧ | D.②⑥⑨ |
D
解析试题分析:A、③该反应是反应前后气体的物质的量不变的反应,所以温度和压强一定时混合气体密度始终不变,④未指明正逆反应,⑤三种物质的浓度比符合系数比时不一定是平衡状态,不能作为平衡状态的标志,错误;B、⑦温度和体积一定时,容器内压强始终不变,⑧ 条件一定,混合气体的平均相对分子质量始终不变,不能作为平衡状态的标志,错误;C、①单位时间内生成n mol H2的同时生成n mol HI,不符合化学方程式中的系数比,错误;D、② 一个H-H键断裂的同时有两个H-I键断裂,⑥ 温度和体积一定时,某一生成物浓度不再变化,符合化学平衡的定义,⑨ 温度和体积一定时混合气体的颜色不再变化,说明碘的浓度不再变化,可以作为平衡状态的标志,正确,答案选D。
考点:考查化学平衡状态的判断

 阅读快车系列答案
阅读快车系列答案工业炼铁是在高炉中进行的,高炉炼铁的主要反应是:① 2C(焦炭)+O2(空气)=2CO;② Fe2O3+3CO=2Fe+3CO该炼铁工艺中,对焦炭的实际使用量要远远高于按照化学方程式计算所需其主要原因是
| A.CO过量 | B.CO与铁矿石接触不充分 |
| C.炼铁高炉的高度不够 | D.CO与Fe2O3的反应有一定限度 |
决定化学反应速率的主要因素是
| A.催化剂 | B.参加反应的物质本身的性质 |
| C.反应物的浓度 | D.温度、压强以及反应物的接触面 |
在温度不变的条件下,在恒容的容器中进行下列反应: 。若
。若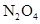 的浓度由
的浓度由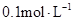 降到
降到 需要15s,那么
需要15s,那么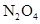 的浓度由
的浓度由 降到
降到 所需的反应时间( )
所需的反应时间( )
| A.等于5s | B.等于10s | C.大于10s | D.小于10s |
一定条件下,可逆反应:X(g) + 3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),反应达到平衡时, X、Y、Z的浓度分别为0.1mol?L-1、0.3 mol?L-1、0.08 mol?L-1,则下列判断不正确的是 ( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),反应达到平衡时, X、Y、Z的浓度分别为0.1mol?L-1、0.3 mol?L-1、0.08 mol?L-1,则下列判断不正确的是 ( )
| A.c1∶c2="=" 1∶3 | B.平衡时,Y和Z生成速率之比为3∶2 |
| C.X、Y的转化率不相等 | D.c1的取值范围为0< c1< 0.14 mol?L-1 |
已知X(g)+3Y(g)═ 2Z(g)△H>0,下列对该反应的说法中正确的是
| A.△S>0 |
| B.逆向能自发进行,且反应速率和平衡常数均较大 |
| C.反应物总能量大于生成物总能量 |
| D.在任何温度下都不能自发进行 |
用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,当反应达到平衡时,下列说法正确的是( )
| A.18O只存在于乙酸乙酯中 | B.18O存在于水、乙酸、乙醇以及乙酸乙酯中 |
| C.18O存在于乙酸乙酯、乙醇中 | D.若与丙酸反应生成酯的相对分子质量为102 |