题目内容
【题目】下列溶液中有关物质的浓度关系正确的是( )
A.1.0 mol/L Na2C2O4溶液中:c(OH﹣)═c(H+)+c(HC2O ![]() )+2c(H2C2O4)
)+2c(H2C2O4)
B.含等物质的量的NaHCO3和Na2CO3的溶液中:3c(Na+)=2[c(HCO ![]() )+c(CO
)+c(CO ![]() )+c(H2CO3)]
)+c(H2CO3)]
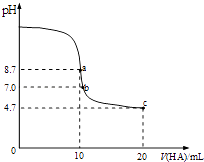
C.二元酸H2A在水中发生电离:H2A=H++HA﹣和HA﹣?H++A2﹣ , 则NaHA溶液中:c(Na+)>c(HA﹣)>c(OH﹣)>c(H+)
D.含有AgCl和AgI固体的悬浊液:c(Cl﹣)<c(I﹣)
【答案】A
【解析】解:A.溶液中存在质子守恒,1.0 mol/L Na2C2O4溶液中:c(OH﹣)═c(H+)+c(HC2O ![]() )+2c(H2C2O4),故A正确; B.含等物质的量的NaHCO3和Na2CO3的溶液中,溶液中存在物料守恒,2n(Na)=3n(C),2c(Na+)=3[c(HCO
)+2c(H2C2O4),故A正确; B.含等物质的量的NaHCO3和Na2CO3的溶液中,溶液中存在物料守恒,2n(Na)=3n(C),2c(Na+)=3[c(HCO ![]() )+c(CO
)+c(CO ![]() )+c(H2CO3)],故B错误;
)+c(H2CO3)],故B错误;
C.分析可知第一步完全电离,HA﹣离子不水解,只电离溶液显酸性,则NaHA溶液中:c(Na+)>c(HA﹣)>c(H+)>c(OH﹣),故C错误;
, D.含有AgCl和AgI固体的悬浊液,碘化银的溶解度小于氯化银,则氯离子浓度大于碘离子,溶液中离子浓度大小为:c(Ag+)>c(Cl﹣)>c(I﹣),故D错误;
故选A.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目