题目内容
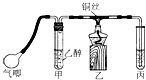
【题目】LiFePO4电池具有稳定性高、安全、对环境友好等优点.某电极的工作原理如图1所示,该电池电解质为能传导 Li+的固体材料.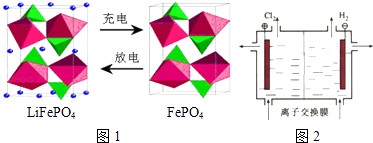
(1)放电时,该电极为极,电极反应为
(2)充电时该电极连接外接电源的极
(3)放电时,电池负极的质量(减少、增加、不变)
(4)LiOH可做制备锂离子电池电极的材料,利用如图2装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.阴极区电解液为溶液(填化学式),离子交换膜应使用(阳、阴)离子交换膜.
【答案】
(1)正;FePO4+e﹣+Li+=LiFePO4
(2)正
(3)减少
(4)LiOH;阳
【解析】解:(1)放电时,该装置是原电池,Fe元素化合价由+3价变为+2价,得电子发生还原反应,所以该电极是正极,电极反应式为FePO4+e﹣+Li+=LiFePO4 , 所以答案是:正;FePO4+e﹣+Li+=LiFePO4;(2)充电时LiFePO4生成FePO4 , 被氧化,应连接电源的正极,所以答案是:正极;(3)放电时,FePO4被还原而消耗,则电极质量减少,所以答案是:减少;(4)电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液,由图可知,右侧生成氢气,则氢离子放电,可知为阴极,制备LiOH,Li+由左侧经过阳离子交换膜向右侧电极移动,应为阳离子交换膜,所以答案是:LiOH;阳.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目