题目内容
下表所列是元素周期表部分短周期的主族元素
| | W | X | Y | |
| R | | | | Z |
已知R为地壳中含量最多的金属元素。
(1)写出Z的原子结构示意图________。
(2)W与氢原子形成6原子分子的结构简式_______。
(3)超细RX粉末被应用于大规模集成电路领域。其制作原理为R2Y3、X2、W在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1∶1;其反应的化学方程式为_______。
(4)X最高价氧化物对应水化物与X气态氢化物反应的生成物溶于水中,所得溶液离子浓度从大到小的顺序是_______。
(5)火箭发动机的燃料胼(N2H4)与氧化剂N2O4反应生成N2和水蒸气。
已知①N2(g)+2O2(g)=N2O4(l) △H1=—195kJ?mol—1
②N2H4(l) +O2(g)=N2(g)+2H2O(g) △H2=—534.2kJ?mol—1
写出肼和N2O4反应的热化学方程式______________。
(6)温度为T时,向2.0L恒容密闭容器中充入1.00 mol PCl5,反应PCl5(g)
 PCl3(g)+Cl2(g),经过一段时间(t)后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g),经过一段时间(t)后达到平衡。反应过程中测定的部分数据见下表:| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
相同温度下,起始时向容器中充入1.00 mol PC15、0.20 mol PCl3和0.40 mol Cl2,反应达到平衡前v(正) _______v(逆)(填“>”或“=”或“<”);原因是_______。
(15分)
(1)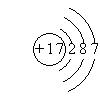 (2分)
(2分)
(2)CH2=CH2 (2分)
(3)Al2O3+N2+3C 2AlN+3CO(3分)
2AlN+3CO(3分)
(4)c(NO3—)>c(NH4+)>c(H+)>c(OH-) (顺序错,漏均不得分)(2分)
(5)2N2H4(l) + N2O4(l)= 3N2(g) + 4H2O(g) ΔH="—873.4" kJ/mol(3分)
(6) <(1分)
因为Qc=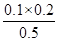 >K=
>K= 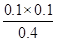 ;所以逆反应速率大于正反应速率。(2分)
;所以逆反应速率大于正反应速率。(2分)
解析试题分析:(1)地壳中含量最多的金属元素是Al,则R、W、X、Y、Z分别是铝、碳、氮、氧、氯,Cl原子核内核电荷数为+17,核外电子层结构为287;(2)碳和氢形成烃,6原子烃分子为乙烯,乙烯的结构简式为CH2=CH2;(3)根据题意,Al2O3、N2、C在高温下反应,可以生成AlN、CO,则反应式为Al2O3+N2+3C 2AlN+3CO;(4)根据题意,HNO3与NH3反应,生成NH4NO3,NH4NO3是盐,根据电解质的电离、盐类水解规律可知,溶液中c(NO3—)>c(NH4+)>c(H+)>c(OH-);(5)根据盖斯定律,由②×2—①可得,2N2H4(l) + N2O4(l)= 3N2(g) + 4H2O(g) ΔH="—873.4" kJ/mol;(6)根据图表可知,
2AlN+3CO;(4)根据题意,HNO3与NH3反应,生成NH4NO3,NH4NO3是盐,根据电解质的电离、盐类水解规律可知,溶液中c(NO3—)>c(NH4+)>c(H+)>c(OH-);(5)根据盖斯定律,由②×2—①可得,2N2H4(l) + N2O4(l)= 3N2(g) + 4H2O(g) ΔH="—873.4" kJ/mol;(6)根据图表可知,
PCl5(g) PCl3(g) + Cl2(g)
PCl3(g) + Cl2(g)
各组分的起始浓度(mol?L—1) 0.50 0 0
各组分的变化浓度(mol?L—1) 0.10 0.10 0.10
各组分的平衡浓度(mol?L—1) 0.40 0.10 0.10
平衡时K=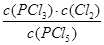 =
=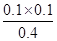
温度不变,平衡常数不变,若起始时充入1.00 mol PC15、0.20 mol PCl3和0.40 mol Cl2,则三者的起始浓度为0.5mol/L、0.10mol/L、0.20mol/L,Q=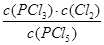 =
=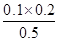 >
>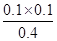 ,说明此时反应必须向逆反应方向进行,才能达到该温度下的化学平衡,所以此时逆反应速率大于正反应速率。
,说明此时反应必须向逆反应方向进行,才能达到该温度下的化学平衡,所以此时逆反应速率大于正反应速率。
考点:考查物质结构和元素周期律、氧化还原反应、质量守恒定律、铝氮碳氧元素及其化合物、盐类水解、电解质溶液中离子浓度大小关系、热化学方程式、盖斯定律、化学平衡的计算与化学反应进行的方向等相关知识。

A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相对位置如图,A元素最外层与次外层上的电子数之差为3,B为地壳中含最最多的金属元素。
| A | |
| | C |
(1)D原子结构示意图为_____________。
(2)将C的低价态氧化物甲通入到D单质的水溶液会使之褪色,体现了甲的________性,写出该反应的离子方程式_____________________。
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到100 mL 8.0 mol/L乙的浓溶液中,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是_________,还原剂失电子数为_________________。
(4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,充分反应生成气体的体积比为__________,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为_____________________________________;B单质表面的氧化膜可用NaOH溶液除去,写出该反应的化学方程式___________________________________。
X、Y、Z、T是元索周期表前四周期中的常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X是地壳中含量最多的元素 |
| Y | Y元素原子核外3p能级上有4个电子 |
| Z | 核素Z的质量数为14、中子数为7 |
| T | T的单质是一种常见的金属,其新制的氢氧化物悬浊液可用于检验糖尿病 |
(2) X的电负性比Y______的 (填“大”或“小”);H-X, H-Y两种共价键中,键长较长的是______(用元素符号表示,下同)。
(3) Z的最高价氧化物对应水化物的稀溶液能与单质T反应,写出该反应的化学方程式,并标出电子转移的 方向和数目: __________________。
(4) 在250C、101 kPa时,若适量的Z2和X2完全反应,每生成30 g ZX需要吸收90 kJ热量。则该反应的热化学方程式为____________。
利用15N可以测定亚硝酸盐对地下水质的污染情况。
(1)下列说法正确的是___。
| A.14N与15N为同种核素 |
| B.14N的第一电离能小于14C |
| C.15NH3与14NH3均能形成分子间氢键 |
| D.CH315NH2与CH3CH214NH2互为同系物 |
(3) 工业上电解法处理亚硝酸盐的模拟工艺如图。

已知:阳极区发生化学反应:
2NO2-+8H++6Fe2+==N2↑ +6Fe3++4HzO
①阳极电极反应方程式是______(不考虑后续反应);
②若硫酸溶液浓度过大,阴极区会有气体逸出,该气体为______(填化学式);该现象表明c( H+ )越大,H+氧化性越______;
③若电解时电路中有0.6 mol电子转移,且NaNO2有剩余,则电解池中生成Na2SO4______mol。
 2EC3(g) △H<0,回答下列问题:
2EC3(g) △H<0,回答下列问题:

 键与π键的数目之比为_________;
键与π键的数目之比为_________;