题目内容
【题目】某学习小组同学根据影响化学反应速率的因素进行实验验证,其设计的实验方案如下:请你帮他们把表填写完整,并做出评价。
(1)甲同学验证还原性:I->Br-
实验步骤 | 实验现象 | 实验结论及离子反应式 |
| 逐滴加入的同时振荡,观察CCl4层的颜色: 甲___ 乙___; 乙中CCl4层颜色明显变化的快。 | 离子方程式: 甲__ 乙__ 结论:验证成立,还原性,I->Br- |
(评价)甲同学设计的实验方案是__(填“合理”或“不合理”),理由是__。
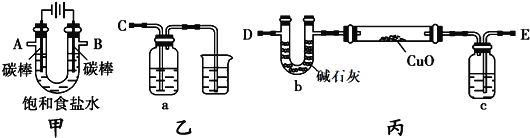
(3)乙同学验证固体反应物的颗粒大小的对反应速率影响
实验步骤:在试管①中加入1g粉末状大理石,加入4mol/L盐酸20mL(过量);在试管②中加入2g颗粒状大理石,加入4mol/L盐酸20mL(过量)。他根据实验过程,绘制出的生成CO2生成体积(折算成标准状况)V(CO2)同反应时间t的关系曲线图,你认为__是符合的。

【答案】橙红色 紫红色 2Brˉ+Cl2=Br2+2Clˉ 2Iˉ+Cl2=I2+2Clˉ 不合理 乙试管中KI溶液的浓度大,反应速率大,现象变化的也快,所以无法得出还原性强弱的结论 D
【解析】
(1)本实验的目的是验证还原性:Iˉ>Brˉ,甲同学的思路是通过比较NaBr溶液、KI溶液分别与氯水反应速率的快慢来确定Iˉ和Brˉ的还原性强弱,控制变量法探究某个问题时要保持变量唯一,甲同学的实验中所用的NaBr溶液和KI溶液的浓度不同,所用并不能达到实验目的。
(2)本实验验证固体反应物的颗粒大小对反应速率影响,粉末状固体接触面积更大,反应速率更快。
(1)氯水中氯气可以氧化溴离子,发生反应2Brˉ+Cl2=Br2+2Clˉ,而溴更易溶于CCl4,所以实验过程中可以观察到甲中CCl4层显橙红色;氯气也可以氧化碘离子,发生反应2Iˉ+Cl2=I2+2Clˉ,碘单质更易溶于CCl4,所以可以观察到CCl4层显紫红色;
甲同学的思路是通过比较NaBr溶液、KI溶液分别与氯水反应速率的快慢来确定Iˉ和Brˉ的还原性强弱,但乙试管中KI溶液的浓度大,反应速率大,现象变化的也快,所以无法得出还原性强弱的结论,甲同学设计的实验方案不合理;
(2)粉末状的大理石与盐酸反应速率更快,所以反应完全之前曲线的斜率更大;但粉末状的大理石只有1g,颗粒状大理石有2g,盐酸过量,所以颗粒状大理石产生的二氧化碳更多,曲线的终点更高,综上所述D是符合的。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案【题目】根据电子排布三原理,填写下列空白。
(1)基态Mn2+的核外电子排布式为________。
(2)磷原子外围电子排布式为________。
(3)氧元素基态原子核外未成对电子数为________个。
【题目】下表为元素周期表的一部分,请参照元素①——⑨在表中的位置,回答问题
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中⑧是用于半导体材料的元素,其元素符号为____,其在周期表中的位置是____。
(2)②、③、④的原子半径最小是____(填元素符号),其原子结构示意图是____。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是____(填化学式)。
(4)①和③形成的原子个数比为1:1的化合物的电子式为____。
(5)⑤和⑨形成的化合物属于____(填“离子化合物”或“共价化合物”),用电子式表示其形成过程____