题目内容
【题目】CO和H2在工业上常作为重要的化工原料,其混合气称为合成气。工业上CH4—H2O 催化重整是目前大规模制取合成气的重要方法,其原理为:
反应Ⅰ:CH4(g)+H2O(g)![]() CO(g)+3H2(g) H1 = +210kJ/mol
CO(g)+3H2(g) H1 = +210kJ/mol
反应Ⅱ:CO(g)+ H2O(g)![]() CO2(g)+H2(g) H2 =﹣41kJ/mol
CO2(g)+H2(g) H2 =﹣41kJ/mol
(1)CH4(g)、H2O(g)反应生成 CO2(g)、H2(g)的热化学方程式是 ___________________________。
(2)反应Ⅰ达到平衡的标志是(____________)
a.恒温恒容情况下,压强不再改变 b. v(CO):v(H2)=1:3
c.平均相对分子质量不再改变 d.恒温恒容情况下,气体密度不再改变
(3)若容器容积不变,不考虑反应Ⅰ,对反应Ⅱ下列措施可增加 CO 转化率的是(____________)
a.升高温度 b.将 CO2 从体系分离 c.充入 He,使体系总压强增大 d.按原投料比加倍投料
(4)某温度下,对于反应Ⅰ,将 n(H2O)∶n(CH4) = 1∶1 的原料气充入恒容密闭容器中,初始压强为 P0,反应达 平衡时总压强为 P1,则平衡时甲烷的转化率为 ____________________________ (忽略副反应)。
(5)将 1molCH4(g) 和 1molH2O(g)加入恒温恒压的密闭容器中(温度 298K、压强 100kPa),发生反应Ⅰ,不考虑 反应Ⅱ的发生,该反应中,正反应速率 v 正=k 正×p(CH4)×p(H2O) , 逆反应速率 v 逆=k 逆×p(CO)×p3(H2),其中 k 正、k 逆 为速率常数,p 为分压(分压=总压×物质的量分数),则该反应的压强平衡常数 Kp= ____________________________ (以 k 正、k 逆表示)。若 该条件下 k 正=4.4×104kPa-1·s-1,当 CH4 分解 20%时,v 正= ___________________________kPa·s-1(保留两位有效数字)。
【答案】CH4(g)+2H2O![]() CO2(g)+4H2(g) H = +169 kJ/mol AC b
CO2(g)+4H2(g) H = +169 kJ/mol AC b ![]() k正/k逆 4.9×107
k正/k逆 4.9×107
【解析】
(1)根据盖斯定律书写热化学方程式;
(2)反应达到平衡状态时,正反应速率等于逆反应速率,各物质的浓度、体积分数、物质的量分数等物理量不变,据此分析;
(3)增加 CO 转化率,平衡正向移动;
(4)根据反应方程式计算,平衡体系总压为各组分分压之和;
(5)根据正反应速率 v 正=k 正×p(CH4)×p(H2O) , 逆反应速率 v 逆=k 逆×p(CO)×p3(H2)以及Kp=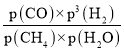 进行计算。
进行计算。
(1)根据盖斯定律反应Ⅰ+反应Ⅱ得:CH4(g)+2H2O![]() CO2(g)+4H2(g) H = +169 kJ/mol;
CO2(g)+4H2(g) H = +169 kJ/mol;
(2)A. 该反应为非等体积反应,压强不再改变,反应达到平衡状态,A项正确;
B.速率之比在任何时候都等于化学计量数之比,不一定是平衡状态,B项错误;
C. 该反应为非等体积反应,平均相对分子质量不再改变, 反应达到平衡状态,C项正确;
D. 反应中质量守恒,气体总质量不变,气体体积不变,密度始终不变,不能证明达到平衡状态,D项错误;
但选AC;
(3)a.该反应为放热反应,升高温度 ,平衡逆向移动,CO 转化率减小,a项错误;
b.将 CO2 从体系分离,减小了生成物的浓度,平衡正向移动,b项正确;
c.充入 He,使体系总压强增大,但各物质的浓度不变,平衡不移动,转化率不变,c项错误;
d.按原投料比加倍投料,新平衡与原平衡等效,转化率不变,d项错误;
答案选b;
(4)设反应中转化的压强为x,则
CH4(g) + H2O(g) ![]() CO(g) + 3H2(g)
CO(g) + 3H2(g)
起始压强 ![]()
![]() 0 0
0 0
转化压强 x x x 3x
平衡压强 ![]() -x
-x ![]() -x x 3x
-x x 3x
![]() -x+
-x+![]() -x+x+3x=P1,解得x=
-x+x+3x=P1,解得x=![]() ,平衡时甲烷的转化率为
,平衡时甲烷的转化率为 ×100%=
×100%=![]() ×100%=(
×100%=(![]() -1) ×100%;
-1) ×100%;
(5)正反应速率 v 正=k 正×p(CH4)×p(H2O) , 逆反应速率 v 逆=k 逆×p(CO)×p3(H2),则p(CH4)×p(H2O)=![]() ,p(CO)×p3(H2)=
,p(CO)×p3(H2)=![]() ,Kp=
,Kp=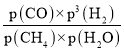 =
=![]() ,达到平衡状态时v(正)=v(逆),因此Kp=
,达到平衡状态时v(正)=v(逆),因此Kp=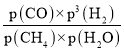 =
=![]() ;当 CH4 分解 20%时,
;当 CH4 分解 20%时,
CH4(g) + H2O(g) ![]() CO(g) + 3H2(g)
CO(g) + 3H2(g)
起始(mol) 1 1 0 0
转化(mol) 0.2 0.2 0.2 0.6
平衡(mol) 0.8 0.8 0.2 0.6
平衡时甲烷的物质的量分数为![]() =
=![]() ,水蒸气的物质的量分数为
,水蒸气的物质的量分数为![]() =
=![]() ,
,
则p(CH4)=100kPa×![]() =
=![]() kPa,p(H2O)= 100kPa×
kPa,p(H2O)= 100kPa×![]() =
=![]() kPa,又v 正=k 正×p(CH4)×p(H2O),当k 正=4.4×104kPa-1·s-1时,v 正=4.4×104×
kPa,又v 正=k 正×p(CH4)×p(H2O),当k 正=4.4×104kPa-1·s-1时,v 正=4.4×104×![]() ×
×![]() =4.9×107 kPa·s-1。
=4.9×107 kPa·s-1。

 阅读快车系列答案
阅读快车系列答案