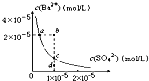题目内容
【题目】把0.6molX气体和0.4molY气体混合于2L容器中,发生反应:3X(g)+Y(g)= nZ(g) +2W(g).5min末已生成0.2molW,若测知以Z浓度的变化来表示平均速率为0.01mol/(L·min),则
(1)上述反应Z气体的计量系数n的值是______;
(2)上述反应在5min末时,已用去的Y占原来物质的质分数是__________。
【答案】1 25%
【解析】
把0.6molX气体和0.4molY气体混合于2L容器中,5min末已生成0.2molW,则:
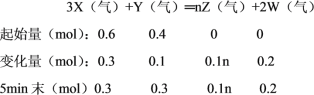
(1)v(Z)=![]() ,计算n;
,计算n;
(2)根据已反应的Y的物质的量占原来量的百分数=![]() ×100%计算.
×100%计算.
把0.6molX气体和0.4molY气体混合于2L容器中,5min末已生成0.2molW,则:
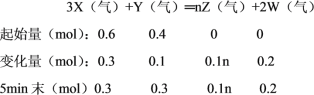
(1)v(Z)=![]() =
=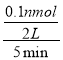 =0.01mol/(L·min),计算n=1;
=0.01mol/(L·min),计算n=1;
(2)根据已反应的Y的物质的量占原来量的百分数=![]() ×100%=
×100%=![]() =25%。
=25%。

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
【题目】下列说法正确的是
A.用坩埚灼烧![]() 的反应式
的反应式 ![]()
![]()
![]()
B.根据表中提供的数据,等物质的量浓度的NaClO、![]() 混合溶液中,有
混合溶液中,有![]()
化学式 | 电离常数 |
HClO |
|
|
|
|
C.常温下,将![]() 的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一
的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一
D.某温度时,![]() 在水中的沉淀溶解平衡曲线如图所示,溶度积常数
在水中的沉淀溶解平衡曲线如图所示,溶度积常数![]() 则加入
则加入![]() 可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点
可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点