题目内容
【题目】下列有机反应方程式书写正确且为加成反应的是( )
A.CH4+Cl2![]() CH2Cl2+H2
CH2Cl2+H2
B.CH2=CH2+Br2→CH3-CHBr2
C.CH2=CH2+H2O![]() CH3CH2OH
CH3CH2OH
D.![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O
【答案】C
【解析】
A. 甲烷和氯气在光照条件下,发生取代反应,生成二氯甲烷和氯化氢,反应方程式为CH4+2Cl2![]() CH2Cl2+2HCl,故A错误;
CH2Cl2+2HCl,故A错误;
B. 乙烯含有碳碳双键,与Br2发生加成反应,生成1,2二溴乙烷,反应方程式为CH2=CH2+Br2→CH2BrCH2Br,故B错误;
C. 乙烯含有碳碳双键,与H2O在催化剂作用下发生加成反应,生成乙醇,反应方程式为CH2=CH2+H2O![]() CH3CH2OH,故C正确;
CH3CH2OH,故C正确;
D. ![]() 和HNO3在浓硫酸、加热的条件下反应,苯环上的氢原子被硝基取代生成硝基苯,苯环应该直接连接氮原子,硝基苯的结构简式书写错误,且该反应为取代反应,故D错误;
和HNO3在浓硫酸、加热的条件下反应,苯环上的氢原子被硝基取代生成硝基苯,苯环应该直接连接氮原子,硝基苯的结构简式书写错误,且该反应为取代反应,故D错误;
故选C。

 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案【题目】化学反应的速率和限度对人类生产生活有重要的意义。
(1)已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响,设计实验如下(所取溶液体积均为2 mL):
实验编号 | 温度/℃ | c(Na2S2O3)/mol·L-1 | c(H2SO4)/mol·L-1 |
Ⅰ | 25 | 0.1 | 0.1 |
Ⅱ | 25 | 0.2 | 0.1 |
Ⅲ | 50 | 0.2 | 0.1 |
①上述实验中溶液最先变浑浊的是______(填实验编号,下同)。
②为探究浓度对化学反应速率的影响,应选择______和______。
(2)某温度下,在1 L密闭容器中,发生反应:2X(g)+Y(g)![]() 2Z(g),X的物质的量随时间的变化如下表:
2Z(g),X的物质的量随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
X的物质的量/mol | 0.02 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
①用X的浓度变化表示0~2 s的平均化学反应速率为______mol/(L·s)。
②在3 s以后X的浓度不再改变,反应达到了______状态。
③能说明该反应已达到化学平衡状态的是______(填序号)。
A.v正(X)=v逆(X)
B.单位时间内有2 mol X生成同时有1 mol Y生成
C.X、Y、Z的分子数之比为2∶1∶2
【题目】下列说法正确的是
A.用坩埚灼烧![]() 的反应式
的反应式 ![]()
![]()
![]()
B.根据表中提供的数据,等物质的量浓度的NaClO、![]() 混合溶液中,有
混合溶液中,有![]()
化学式 | 电离常数 |
HClO |
|
|
|
|
C.常温下,将![]() 的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一
的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一
D.某温度时,![]() 在水中的沉淀溶解平衡曲线如图所示,溶度积常数
在水中的沉淀溶解平衡曲线如图所示,溶度积常数![]() 则加入
则加入![]() 可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点
可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点
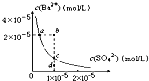
【题目】下表中的实验操作能达到实验目的或能得出相应结论的是![]()
选项 | 实验操作 | 实验目的或结论 |
A | 向一定浓度的 |
|
B | 取少量 | 检验 |
C | 向某溶液中滴加 | 说明原溶液中一定含有 |
D | 将混有 | 除去 |
A.A