题目内容
3.下列叙述正确的是( )| A. | Fe与S混合加热生成FeS2 | |
| B. | NaHCO3的热稳定性大于Na2CO3 | |
| C. | 过量的铜与浓硝酸反应有一氧化氮生成 | |
| D. | Fe在足量Cl2中燃烧生成和FeCl2和FeCl3 |
分析 A.S具有弱氧化性,能将变价金属氧化为较低价态;
B.碳酸氢钠受热易分解生成碳酸钠;
C.过量Cu和浓硝酸反应时先生成二氧化氮后生成NO;
D.氯气具有强氧化性,能将变价金属氧化为较高价态.
解答 解:A.S具有弱氧化性,能将变价金属氧化为较低价态,所以Fe与S混合加热生成FeS,故A错误;
B.碳酸氢钠受热易分解生成碳酸钠,碳酸钠较稳定,所以碳酸钠的稳定性大于碳酸氢钠,故B错误;
C.过量Cu和浓硝酸反应时先生成二氧化氮,随着反应进行,浓硝酸转化为稀硝酸,Cu和稀硝酸反应生成NO,故C正确;
D.氯气具有强氧化性,能将变价金属氧化为较高价态,无论氯气是否过量,铁和氯气反应都生成氯化铁,故D错误;
故选C.
点评 本题考查金属、硝酸、S、氯气的性质,侧重考查元素化合物知识,注意硫氧化性远远小于氯气的氧化性,导致硫和变价金属反应生成较低价态金属硫化物、氯气和变价金属反应生成较高价态金属氯化物,易错选项是D.

练习册系列答案
相关题目
13. 一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
 一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )| A. | 反应的化学方程式为4X?Y | |
| B. | t2时,正反应速率等于逆反应速率 | |
| C. | t3时,Y浓度不再变化,反应达到平衡 | |
| D. | 当t1=2时,用X表示该反应在2 min内的平均反应速率为0.25mol/(L•min) |
14.向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到深蓝色透明溶液.若加入乙醇将析出深蓝色晶体.下列说法正确的是( )
| A. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| B. | 在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤对电子 | |
| C. | 沉淀溶解后将生成深蓝色的正四面体形的配离子[Cu(NH3)4]2+ | |
| D. | 加入极性较小的溶剂乙醇后,将析出[Cu(H2O)4]SO4•H2O晶体 |
11.下列关于化学键和分子间作用力的说法中不正确的是( )
| A. | 化学键是一种作用力 | |
| B. | 化学键可以使离子相结合,也可以使原子相结合 | |
| C. | 一种物质只含两种非金属元素,该物质中一定没有非极性供价键 | |
| D. | 氢键属于分子间作用力,不属于化学键 |
18.下列关于有机物的说法中,正确的是( )
| A. | 用水不能鉴别苯和溴苯 | |
| B. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 | |
| C. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰钾溶液褪色 | |
| D. | 某有机物的分子结构如图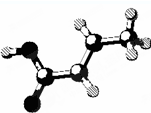 (图中棍表示单键、双键或叁键),它属于烃的含氧衍生物,该有机物可发生取代反应和加成反应 (图中棍表示单键、双键或叁键),它属于烃的含氧衍生物,该有机物可发生取代反应和加成反应 |
8.在25℃时,用蒸馏水稀释1mol/L的醋酸溶液至0.01mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
| A. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ | B. | $\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$ | ||
| C. | $\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$ | D. | $\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$、 |
15.下列实验操作或实验所得出的结论一定正确的是( )
| A. | 制备Fe(OH)3胶体时,应往沸水中逐滴加lmol•L-l的FeCl3溶液,并继续加热到液体呈透明的红褐色为止 | |
| B. | 加热NH4Cl晶体时,用湿润的红色石蕊试纸靠近试管口,检验NH3的生成 | |
| C. | 将金属钠在研钵中研成粉末,使钠与水反应的实验更安全 | |
| D. | 用托盘天平准确称取5.85g NaCl固体 |
12.当下列物质以晶体形式存在时,其所属晶体类型和所含化学键类型分别相同的是( )
| A. | 氯化钠、氯化氢 | B. | 二氧化碳、二氧化硅 | ||
| C. | 四氯化碳、四氯化硅 | D. | 单质铁、单质碘 |
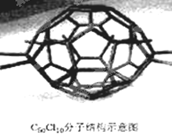
13.厦门大学郑兰荪院士合成了C70Cl10富勒烯足球状分子,如图,它是由C70分子与Cl2发生加成反应得到的.在C70分子中每个碳原子均与周围相邻的其他3个碳原子相连,70个碳原子组成若干个正六边形和正五边形.则有关说法中不正确的是
( )
( )

| A. | C70的熔点比石墨的熔点低 | |
| B. | C70和金刚石是同素异形体 | |
| C. | C70分子中含有70个σ键,35个π键 | |
| D. | C70Cl10分子中共用电子对数目为145个 |