题目内容
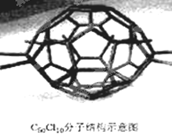
13.厦门大学郑兰荪院士合成了C70Cl10富勒烯足球状分子,如图,它是由C70分子与Cl2发生加成反应得到的.在C70分子中每个碳原子均与周围相邻的其他3个碳原子相连,70个碳原子组成若干个正六边形和正五边形.则有关说法中不正确的是( )
| A. | C70的熔点比石墨的熔点低 | |
| B. | C70和金刚石是同素异形体 | |
| C. | C70分子中含有70个σ键,35个π键 | |
| D. | C70Cl10分子中共用电子对数目为145个 |
分析 A.C70属于分子晶体,熔点低于混合型晶体石墨;
B.同种元素形成的结构不同的单质互为同素异形体;
C.在C70分子中每个碳原子均与周围相邻的其他3个碳原子相连,每个碳原子有四个未成对电子,分别和其他三个原子形成碳碳键,四对公用电子对,有一条键是双键,因此双键个数是70÷2=35,则单键个数是(70×4-35×4)÷2=70.由于双键是由1个σ键和1个π键构成的;
D.计算C70Cl10分子中原子最外层电子总数,每2个电子形成1对共用电子对.
解答 解:C70是由碳元素组成的单质,属于分子晶体,熔点低于石墨的,故A正确;
B.C70和金刚石都是碳元素形成的不同单质,互为同素异形体,故B正确;
C.在C70分子中每个碳原子均与周围相邻的其他3个碳原子相连,每个碳原子有四个未成对电子,分别和其他三个原子成键碳碳键,四对公用电子对,所以,必然有一条键是双键,因此双键个数是70÷2=35,则单键个数是(70×4-35×4)÷2=70.由于双键是由1个σ键和1个π键构成的,则C70分子中含有105个σ键,35个π键,故C错误;
D.C70Cl10分子中共用电子对数目为(70×4+10)÷2=145,故D正确,
故选C.
点评 本题综合性强,对学生的要求较高,有利于激发学生的学习兴趣和学习积极性,有利于培养学生的逻辑推理能力和抽象思维能力,难度中等.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
3.下列叙述正确的是( )
| A. | Fe与S混合加热生成FeS2 | |
| B. | NaHCO3的热稳定性大于Na2CO3 | |
| C. | 过量的铜与浓硝酸反应有一氧化氮生成 | |
| D. | Fe在足量Cl2中燃烧生成和FeCl2和FeCl3 |
4.下列离子方程式书写错误的是( )
| A. | 向足量的NaHCO3溶液中逐渐滴入澄清石灰水:Ca2++2OH-+2HCO3-═2H2O+CaCO3↓+CO32- | |
| B. | 向足量的NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液:Ba2++2H++2HCO3-+SO42-═2H2O+BaSO4↓+2 CO2↑ | |
| C. | 向饱和Na2CO3溶液中通入足量的CO2:CO32-+CO2+H2O═2HCO3- | |
| D. | 向NaHSO4溶液中逐渐滴入Ba(OH)2溶液至沉淀完全:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
1.在一定温度下,向饱和苛性钠溶液中加入一定量的过氧化钠,充分反应后恢复到原温度,下列有关说法中,正确的是( )
| A. | 溶液中Na+浓度增大,有O2放出 | B. | 溶液的碱性不变,有H2放出 | ||
| C. | 溶液中Na+数目减少,有O2放出 | D. | 溶液的碱性不变,有O2放出 |
18.为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
| 物质 | 试剂 | 分离方法 | |
| ① | 甲烷(乙烯) | 高锰酸钾溶液 | 洗气 |
| ② | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
| ③ | 乙醇(水) | 生石灰 | 蒸馏 |
| ④ | 苯(苯酚) | 浓溴水 | 过滤 |
| A. | ②③ | B. | ①③ | C. | ①② | D. | ①④ |
5.最近我国接连发生多起煤矿爆炸事故,造成重大人员伤亡和财产损失.煤矿发生爆炸事故的元凶是煤矿坑道气中含有的甲烷.下列关于甲烷的叙述中错误的是( )
| A. | 甲烷分子是一种呈正四面体型的、含极性键的非极性分子 | |
| B. | 甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子 | |
| C. | 甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业 | |
| D. | “抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸 |
2.已知aAn+,bB(n+1)+,cCn-,dD(n+1)-是具有相同的电子层结构的短周期元素形成的简单离子,下列叙述正确的是( )
| A. | 最外层电子数:C>D>A>B | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:Cn->D(n+1)->An+>B(n+1)+ | D. | 单质还原性:B>A>C>D |
3.NA是阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.00mol NaCl中含有NA个NaCl分子 | |
| B. | 1.00mol NaCl中,所有Na+的最外层电子总数为8NA | |
| C. | 欲配制1.00L,1.00mol•L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 | |
| D. | 标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA |