题目内容
【题目】I.甲醛在木材加工、医药等方面有重要用途。甲醇直接脱氢是工业上合成甲醛的新方法,制备过程涉及的主要反应如下:
反应I:CH3OH(g) ![]() HCHO(g)+H2(g) △H1
HCHO(g)+H2(g) △H1
反应II:CH3OH(g)+1/2O2(g) ![]() HCHO(g)+H2O(g) △H2= —156.6kJ/mol
HCHO(g)+H2O(g) △H2= —156.6kJ/mol
反应III:2H2(g)+O2(g) ![]() 2H2O(g) △H3= —483.6kJ/mol
2H2O(g) △H3= —483.6kJ/mol
(1)计算反应I的反应热△H1=_____________。
(2)750K下,在恒容密闭容器中,发生反应CH3OH(g) ![]() HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=___________(用含P0和α的式子表示);当P0=101kPa,测得α=50.0%,计算反应平衡常数Kp=___________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=___________(用含P0和α的式子表示);当P0=101kPa,测得α=50.0%,计算反应平衡常数Kp=___________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
II. CO2既是温室气体,也是重要的化工原料,以CO2为原料可合成多种有机物。
(3)二氧化碳与氢气在催化剂作用下可制取低碳烯烃。在一恒容密闭容器中分别投入1molCO2、3molH2,发生反应:2CO2(g)+6H2(g) ![]() C2H4(g)+4H2O(g) △H;在不同温度下,用传感技术测出平衡时H2的物质的量变化关系如图所示。
C2H4(g)+4H2O(g) △H;在不同温度下,用传感技术测出平衡时H2的物质的量变化关系如图所示。

①其他条件不变,起始时若按1molCO2、2molH2进行投料,则CO2的转化率将________(填“增大”“ 减小”或“不变”)。
②△H______ (填“>”“<”或“不能确定”)0。
③若测试中体系内无氧气产生,试结合图示推断热稳定性:C2H4_________(填“>” “<”或“不能
确定”)H2O。
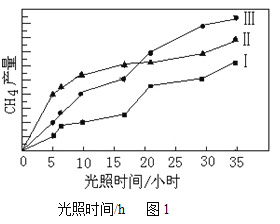
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化见图1。在15小时内,CH4的平均生成速率I、Ⅱ和Ⅲ从大到小的顺序为______________(填序号)。
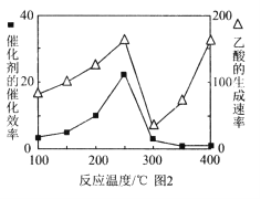
(5)以 TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图2。乙酸的生成速率主要取决于温度影响的范围是______________________。
【答案】+85.2kJ·mol-1 p0(1+a) 50.5kPa 减小 < < v(Ⅱ)>v(Ⅲ)>v(Ⅰ) 300℃~400℃
【解析】
(1)根据盖斯定律进行计算△H2;
(2)根据三段式进行分析计算;压强之比等于物质的量之比,根据平衡常数Kp= ![]() 进行计算;
进行计算;
(3)①其它条件不变,起始时若按1molCO2、2 molH2进行投料,与原平衡相比,相当于减小氢气的浓度,据此分析CO2的转化率变化情况;
②△H只与温度有关,由图升高温度,氢气的量增加,平衡逆向移动,正反应放热;
③若测试中体系内无氧气产生,结合图示温度高于TA℃时,n(H2)大幅提高,说明C2H4受热分解生成氢气,进而推断C2H4和H2O热稳定性大小;
(4)由图2可知,在0~15h内,甲烷的物质的量变化量为△n(Ⅱ)>△n(Ⅲ)>△n(Ⅰ),从而计算0~15h内,CH4的平均生成速率,进而比较大小;在不同催化剂(I、Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化,由图1可得:在15小时内,甲烷的物质的量变化量为△n(Ⅱ)>△n(Ⅲ)>△n(Ⅰ),据此判断CH4的平均生成速率;
(5)在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图2。温度超过250℃时,催化剂的催化效率降低,在300℃时失去活性,所以温度高于300℃时,乙酸的生成速率升高是由温度升高导致的,据此进行分析。
(1)反应I:CH3OH(g) ![]() HCHO(g)+H2(g) △H1
HCHO(g)+H2(g) △H1
反应II:CH3OH(g)+1/2O2(g) ![]() HCHO(g)+H2O(g) △H2= —156.6kJ/mol
HCHO(g)+H2O(g) △H2= —156.6kJ/mol
反应III:2H2(g)+O2(g) ![]() 2H2O(g) △H3= —483.6kJ/mol
2H2O(g) △H3= —483.6kJ/mol
根据盖斯定律,反应I=反应Ⅱ-反应III,计算反应I的反应热△H1=—156.6kJ/mol-(—483.6kJ/mol)=+85.2kJ·mol-1;
(2)若起始压强为P0,达到平衡转化率为α,
CH3OH(g)![]() HCHO(g)+H2(g)
HCHO(g)+H2(g)
起始(mol) 1 0 0
变化(mol) a a a
平衡(mol) 1-a a a
压强之比等于物质的量之比,则p0:P平=1:(1+a),P平=p0(1+a);当P0=101kPa,测得α=50.0%,该反应平衡常数Kp=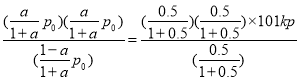 =50.5kPa;
=50.5kPa;
(3)①其他条件不变,起始时若按1molCO2、2 molH2进行投料,与原平衡相比,相当于减小氢气的浓度,则CO2的转化率将减小;
②△H只与温度有关,由图升高温度,氢气的量增加,平衡逆向移动,正反应放热,△H<0;
③若测试中体系内无氧气产生,结合图示温度高于TA℃时,n(H2)大幅提高,说明C2H4受热分解生成氢气,推断热稳定性:C2H4<H2O;
(4)由图2可知,在0~15h内,甲烷的物质的量变化量为△n(Ⅱ)>△n(Ⅲ)>△n(Ⅰ),故在0~15h内,CH4的平均生成速率v(Ⅱ)>v(Ⅲ)>v(Ⅰ);在不同催化剂(I、Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化,由图1可得:在15小时内,甲烷的物质的量变化量为△n(Ⅱ)>△n(Ⅲ)>△n(Ⅰ),CH4的平均生成速率I、Ⅱ和Ⅲ从大到小的顺序为v(Ⅱ)>v(Ⅲ)>v(Ⅰ)。
(5)在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图2。温度超过250℃时,催化剂的催化效率降低,在300℃时失去活性,所以温度高于300℃时,乙酸的生成速率升高是由温度升高导致的,故乙酸的生成速率主要取决于温度影响的范围是300℃~400℃。