题目内容
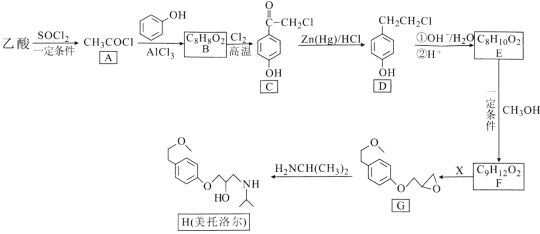
【题目】某同学拟用A、C两种有机物合成F(苯乙酸乙酯),合成的路线如图所示:
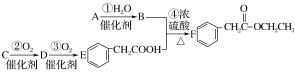
已知:A为最简单的烯烃,C为烃的衍生物,D中含有—CHO。
(1)请写出C的结构简式:________________。
(2)请写出①④的反应类型:①_______________④______________。
(3)请分别写出C、E中官能团的名称:C___________E__________。
(4)写出反应②④的化学方程式:
②__________;
④_________。
(5)J是有机物A的同系物,且比A多1个碳原子,J的加聚产物的结构简式______________。
【答案】 加成反应 酯化反应(或取代反应) 羟基 羧基 2
加成反应 酯化反应(或取代反应) 羟基 羧基 2![]() +O2
+O2![]() 2
2![]() +2H2O
+2H2O ![]() +CH3CH2OH
+CH3CH2OH![]()
![]() +H2O
+H2O 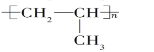
【解析】
A为最简单的烯烃,则A为CH2=CH2,乙烯与水发生加成反应得B为CH3CH2OH,B与E发生酯化(取代)反应生成F,C经过两步氧化得E,D中含有-CHO,由E的结构简式可知,D为![]() ,C为
,C为![]() 。
。
(1)根据以上分析可知C为![]() ,故答案为:
,故答案为: ![]() ;
;
(2)反应①是乙烯和水加成生成乙醇;反应②为![]() 被催化氧化生成
被催化氧化生成![]() ,即
,即![]()
![]() ;反应④为
;反应④为![]() 与CH3CH2OH发生的酯化反应,即
与CH3CH2OH发生的酯化反应,即![]()
![]() ,根据上面的分析可知,反应①为加成反应,反应④为酯化反应(或取代反应),故答案为:加成反应;酯化反应(或取代反应);
,根据上面的分析可知,反应①为加成反应,反应④为酯化反应(或取代反应),故答案为:加成反应;酯化反应(或取代反应);
(3)根据E的结构简式可知,E中含有羧基,C为![]() ,则C中含有羟基,故答案为:羟基;羧基;
,则C中含有羟基,故答案为:羟基;羧基;
(4)反应②的化学方程式为2![]() +O2
+O2![]() 2
2![]() +2H2O,反应④的化学方程式为
+2H2O,反应④的化学方程式为![]() +CH3CH2OH
+CH3CH2OH![]()
![]() +H2O,故答案为:2
+H2O,故答案为:2![]() +O2
+O2![]() 2
2![]() +2H2O;
+2H2O;![]() +CH3CH2OH
+CH3CH2OH![]()
![]() +H2O;
+H2O;
(5) J是有机物A的同系物,且比A多1个碳原子,则J为CH2=CH-CH3,则J的加聚产物的结构简式为:![]() ,故答案为:
,故答案为:![]() 。
。

【题目】下列是25 ℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
Ksp或Ka | Ksp=1.8×10-10 | Ksp=9.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
A. H2CO3、HCO3-、CH3COO-、ClO- 在溶液中可以大量共存
B. 等体积等浓度的CH3COONa和NaClO中离子总数:CH3COONa <NaClO
C. 向浓度均为1.0×10-3 mol·L-1的KCl和K2CrO4混合溶液中滴加1.0×10-3 mol·L-1的AgNO3溶液,CrO42―先形成沉淀
D. 向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液中至c(CH3COOH):c(CH3COO-)=5∶9,此时溶液的pH=5