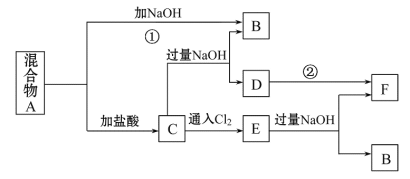
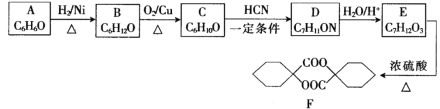
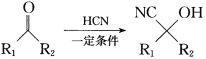
题目内容
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.常温常压下,11.2LCO2所含的原子数为1.5NA
B.常温下,46gNO2和N2O4的混合物中含有的氮原子数为NA
C.1L0.5mol·L-lFeCl3溶液完全转化可制得0.5NA个Fe(OH)3胶粒
D.1molNa被完全氧化生成Na2O2,失去2NA个电子
【答案】B
【解析】
A.常温常压下不能用气体摩尔体积计算CO2物质的量,则所含的原子数不为1.5NA,故A错误;
B.NO2和N2O4的最简式均为NO2,故46g混合物中含有的NO2的物质的量n=![]() =1mol,故含氮原子数即NA个,故B正确;
=1mol,故含氮原子数即NA个,故B正确;
C.胶体是小分子的集合体,则1L0.5mol·L-lFeCl3溶液完全转化可制得Fe(OH)3胶粒数目小于0.5NA个,故C错误;
D.Na2O2中Na为+1价,1molNa被完全氧化生成Na2O2,失去NA个电子,故D错误;
答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的反应:![]()
![]() 下表所列数据是该反应在不同温度下的化学平衡常数
下表所列数据是该反应在不同温度下的化学平衡常数![]() .
.
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断反应I为 ______ 热反应(填“吸”或“放”) ![]() 某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得
某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得![]() ,则CO的转化率为 ______ ,此时的温度为 ______ 从表中选择.
,则CO的转化率为 ______ ,此时的温度为 ______ 从表中选择.
(2)已知在常温常压下:
①![]()
②![]()
③![]()
则反应![]() ______
______ ![]() 用
用![]() 、
、![]() 、
、![]() 表示
表示
(3)处理废水时,最后![]() 以
以![]() 形式除去,当
形式除去,当![]() 时,
时,![]() 沉淀完全,此时溶液的
沉淀完全,此时溶液的![]() ______ (已知,
______ (已知,![]() ,
,![]() )
)