题目内容
9.下列叙述错误的是( )| A. | 用灼烧的方法可以鉴别羊毛和棉花 | |
| B. | 用饱和碳酸钠溶液除去乙酸乙酯中的乙酸 | |
| C. | 用酒精清洗沾到皮肤上的苯酚 | |
| D. | 用酸性高猛酸钾溶液鉴别甲苯和苯乙烯 |
分析 A.羊毛的主要成分为蛋白质,可灼烧;
B.乙酸乙酯不溶于饱和碳酸钠,乙酸与碳酸钠反应;
C.苯酚易溶于酒精;
D.甲苯和苯乙烯都可被酸性高锰酸钾氧化.
解答 解:A.羊毛的主要成分为蛋白质,灼烧时具有烧焦的羽毛气味,棉花的主要成分为纤维素,可鉴别,故A正确;
B.乙酸乙酯不溶于饱和碳酸钠,乙酸与碳酸钠反应,可用于饱和碳酸钠溶液分离,故B正确;
C.苯酚易溶于酒精,可用酒精洗涤,故C正确;
D.甲苯和苯乙烯都可被酸性高锰酸钾氧化,应用溴水鉴别,故D错误.
故选D.
点评 本题考查有机物的鉴别,为高频考点,侧重于有机物的结构、性质的考查,注意把握有机物的性质的异同以及检验、鉴别的方法,难度不大.

练习册系列答案
相关题目
20.下列实验装罝、操作或现象描述正确的是( )
| A. | 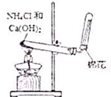 实验室制取NH3 | B. | 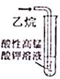 溶液颜色褪去 | C. | 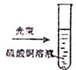 看到光亮的通路 | D. | 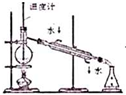 石油蒸馏 |
17.常温下,向pH=2的醋酸溶液中加入少量0.01mol•L-1的盐酸,溶液中一定发生变化的是( )
| A. | c(CH3COO-) | B. | KW | C. | Ka(CH3COOH) | D. | c(H+) |
4.乙酸乙酯广泛存在于菠萝、香蕉等果品中.实验室制备乙酸乙酯的有关信息如表,装置如图1所示.
实验方案如图2所示.
(1)仪器B的名称是球形冷凝管.
(2)制取乙酸乙酯的化学方程式为CH3COOH+C2H5OH$→_{△}^{浓硫酸}$CH3COOC2H5+H2O.
(3)本实验采取先回流后蒸馏的优点是减少乙醇蒸发,提高酯的产量.
(4)馏分用饱和的Na2CO3溶液洗涤是为了除去乙酸和乙醇.
(5)馏分用饱和的NaCl溶液洗涤是为了除去除去碳酸钠或醋酸钠或乙醇或水(填一种),酯在分流漏斗的上(填“上”或“下”)层.
(6)经洗涤的馏分加入少量无水MgSO4固体的作用是除去水分.
(7)经以上分离操作后,产品中还含有的杂质是乙醇,需进一步进行的提纯操作是d(填字母).
a.过滤 b.重结晶 c.萃取 d.精细蒸馏
(8)经进一步提纯后,得乙酸乙酯13.2g,则产率为71.4%.
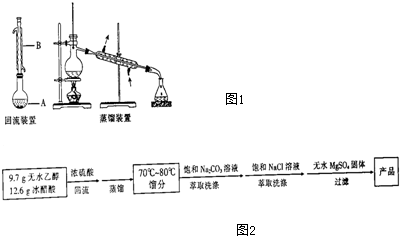
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解度 | |
| 乙醇 | 46 | 0.789 | 78.3 | 溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸乙酯 | 88 | 0.897 | 77 | 微溶 |
(1)仪器B的名称是球形冷凝管.
(2)制取乙酸乙酯的化学方程式为CH3COOH+C2H5OH$→_{△}^{浓硫酸}$CH3COOC2H5+H2O.
(3)本实验采取先回流后蒸馏的优点是减少乙醇蒸发,提高酯的产量.
(4)馏分用饱和的Na2CO3溶液洗涤是为了除去乙酸和乙醇.
(5)馏分用饱和的NaCl溶液洗涤是为了除去除去碳酸钠或醋酸钠或乙醇或水(填一种),酯在分流漏斗的上(填“上”或“下”)层.
(6)经洗涤的馏分加入少量无水MgSO4固体的作用是除去水分.
(7)经以上分离操作后,产品中还含有的杂质是乙醇,需进一步进行的提纯操作是d(填字母).
a.过滤 b.重结晶 c.萃取 d.精细蒸馏
(8)经进一步提纯后,得乙酸乙酯13.2g,则产率为71.4%.

14.为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是( )
| 选项 | 实验目的 | 主要仪器 | 试剂 |
| A | 分离Br2和CCl4混合物 | 分液漏斗、烧杯 | Br2和CCl4混合物、蒸馏水 |
| B | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液、水 |
| C | 实验室制取H2 | 试管、带导管的橡皮塞 | 锌粒、稀HNO3 |
| D | 除去CH4中的C2H4 | ]试管、带导管的橡皮塞 | 酸性KMnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
1.化学与资源、环境、生活关系密切,下列说法正确的是( )
| A. | 燃烧汽油产生的汽车尾气中所含的大气污染物主要是CO,NO、SO2、CO2等 | |
| B. | 乙醇、次氯酸钠溶液均可以将病毒氧化而消毒 | |
| C. | 用纯碱溶液清洗餐具上的油污时,加热可以提高去污能力 | |
| D. | 火力发电是将化学能直接转化为电能 |
18.以下化学用语正确的是 ( )
| A. | Cr最外层电子排布式 4s2 | B. | 乙醇的结构简式CH3CH2OH | ||
| C. | 二氧化硅的分子式 SiO2 | D. | 甲醛的电子式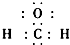 |
19.关于下列实验,说法正确的是( )
| A. | 将一块铝片投入足量NaOH溶液中,充分反应后铝片消失,将溶液蒸干便可得到纯净NaAlO2 | |
| B. | 将二块相同铝片投入到等物质的量浓度的CuSO4和CuCl2溶液中,反应速率几乎相同 | |
| C. | 将铝粉投入浓NaOH溶液中,1mol铝可还原3mol水 | |
| D. | 将一小块钠投入盛有乙醇的烧杯中,由于钠的密度大于乙醇,所以钠一直在液面下反应 |
 .
.