题目内容
12.已知H2O2的分子空间结构可在二面角中表示,如图所示,则有关H2O2的结构的说法中正确的是( )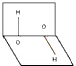
| A. | 分子的正、负电荷重心重合 | B. | 分子正、负电荷重心不重合 | ||
| C. | H2O2是极性分子 | D. | H2O2是非极性分子 |
分析 根据图象知,双氧水分子的正负电荷重心不重合;正负电荷重心不重合的分子为极性分子;据此分析.
解答 解:A、双氧水分子空间构型是二面角构型,所以正负电荷重心不重合,故A错误;
B.双氧水分子空间构型是二面角构型,所以正负电荷重心不重合,故B正确;
C.根据图象知,该分子正负电荷重心不重合,为极性分子,故C正确;
D.根据图象知,该分子正负电荷重心不重合,为极性分子,故D错误;
故选BC.
点评 本题考查了分子极性、化学键的判断,根据其空间构型分析解答,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列物质中最难电离出H+的是( )
| A. | C6H5OH | B. | H2O | C. | HNO3 | D. | C2H5OH |
17.有一瓶K2SO3溶液,由于它可能部分被氧化,某同学进行如下实验:取少量样品溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀.对此实验下述结论正确的是( )
| A. | K2SO3已部分被空气中的氧气氧化 | |
| B. | 加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4 | |
| C. | 加硝酸后的不溶性沉淀中含有BaSO3 | |
| D. | 此实验不能确定K2SO3是否部分被氧化 |
2.下列关于元素周期表的叙述,不正确的是( )
| A. | 共有7个周期,16个族 | |
| B. | 形成化合物种类最多的元素在第2周期 | |
| C. | 第ⅡA族的右边是第ⅢB族,第ⅢA族的左边是第ⅡB族 | |
| D. | 某主族元素最高价氧化物对应的水化物的化学式为HnROm,其气态氢化物的化学式一定为H2m-nR或RH2m-n |
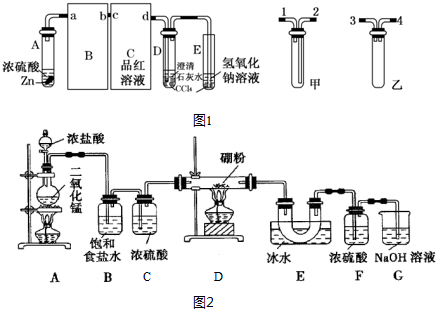
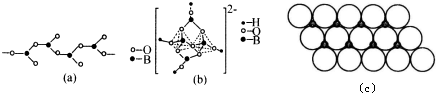
 使用如图所示装置进行化学小实验,请填写下列空白:
使用如图所示装置进行化学小实验,请填写下列空白: