题目内容
【题目】(1)铁元素是构成人体的必不可少的元素之一,缺铁会影响到人体的健康和发育,最大的影响是缺铁性贫血。此类病人需要服用补铁药品。

一个体重50 kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是________。
A.Fe B.Fe2+ C.Fe3+
(2)亚硝酸钠有毒,有传言说亚硝酸钠是致癌物质,但事实上亚硝酸钠并不是致癌物质,致癌的是亚硝酸钠在一定条件下生成的亚硝胺。工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有_______性。下列不能实现上述转化的物质是_______。
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了________性和________性,则生成1分子NO转移电子数为________;56g Fe参加反应时,被还原的HNO3为________g。
【答案】B 氧化 C 酸 氧化 3个 63
【解析】
(1)最高价态的粒子只有氧化性,最低价态的粒子只有还原性,中间价态的粒子既有氧化性又有还原性;
(2)Fe2+→Fe3+发生了氧化反应,NaNO2具有氧化性,所以实现此转化也应选择具有强氧化性的物质,而FeCl3与Fe2+不能反应,FeCl3不能实现上述转化;
(3)Fe和HNO3的反应中,一部分HNO3起氧化作用,生成NO,另一部分则起酸性作用生成Fe(NO3)3,所以56gFe参加反应时,只有1molHNO3被还原。
(1)最高价态的粒子只有氧化性,最低价态的粒子只有还原性,中间价态的粒子既有氧化性又有还原性,在Fe、Fe2+、Fe3+中,既有氧化性又有还原性的是Fe2+,故合理选项是B;
(2)Fe2+→Fe3+发生了氧化反应,说明NaNO2具有氧化性,所以实现此转化也应选择具有强氧化性的物质,而FeCl3与Fe2+不能反应,因此FeCl3不能实现上述转化,Cl2 、O2、KMnO4(H+)都具有强的氧化性,可以将Fe2+氧化为Fe3+。故合理选项是C;
(3)在反应Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O中,HNO3一部分起氧化作用,生成NO,另一部分则起酸性作用生成Fe(NO3)3,每产生1分子的NO,元素化合价改变了3价,反应转移电子数目为3个。56gFe的物质的量是1mol,当1molFe参加反应时,只有1mol硝酸被还原,所以被还原HNO3的质量为1mol×63g/mol=63g。

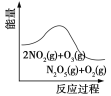
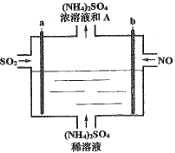
【题目】臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO2(g)+O3(g) ![]() N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A | B | C | D |
|
|
|
|
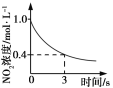
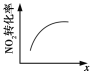
升高温度,平衡常数减小 | 0~3 s内,反应速率为:v(NO2)=0.2 mol·L-1 | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
A. AB. BC. CD. D
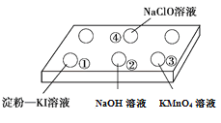
【题目】把浓盐酸分别滴入点滴板上的各种溶液中,现象如下:
实验 | 现象 |
| ①中溶液变蓝且无其他明显现象 |
②中无明显现象 | |
③中溶液褪色 | |
④中产生黄绿色气体 |
下列分析正确的是( )
A.①中现象体现了浓盐酸的氧化性
B.②中现象说明未发生反应
C.③中反应后氯元素全部以KCl形式存在
D.④中产生黄绿色气体的反应是:ClO-+ Cl-+ 2H+ = Cl2↑+ H2O