题目内容
【题目】利用反应 NO2+NH3→N2+H2O(未配平)制作下面装置图所示的电池,用以消除氮氧化物的污染。下列有关该电池说法一定正确的是 ( )

A.电极乙为电池负极
B.离子交换膜为质子交换膜
C.负极反应式为 2NH3-6e-+6OH-=N2↑+6H2O
D.28.0L(标准状况)NO2 完全被处理,转移 4mol 电子
【答案】C
【解析】
根据题干信息,反应NO2+NH3→N2+H2O中,NO2中N元素化合价降低,得到电子,发生还原反应,NH3中N元素化合价升高,失去电子,发生氧化反应,则电极甲为负极,电极乙为正极,据此分析解答。
A.由上述分析可知,电极乙为原电池的正极,A选项错误;
B.该电池中,NO2在正极得到电子,发生还原反应,电极反应式为2NO2+4H2O+8e-===N2+8OH-,OH-向负极移动,则离子交换膜为阴离子交换膜,B选项错误;
C.NH3在负极失去电子,发生氧化反应,电极反应式为2NH3-6e-+6OH-=N2↑+6H2O,C选项正确;
D.由负极反应2NO2+4H2O+8e-===N2+8OH-,转移4mol电子需处理1molNO2,标准状况下NO2为液体,28.0L的物质的量未知,D选项错误;
答案选C。

【题目】氮的化合物在工农业生产及航天航空业中具有广泛的用途。回答下列问题:
⑴NF3为无色、无味的气体,可用于微电子工业,该物质在潮湿的环境中易变质生成HF、NO、HNO3。该反应中氧化剂与还原剂的物质的量之比为______,NF3在空气中泄漏时很容易被观察到,原因是_______。
⑵汽车尾气中催化剂可将NO、CO转化成无害气体。
化学键 | C≡O | NO中氮氧键 | N≡N | CO2中C=O键 |
键能/kJ·mol1 | 1076 | 630 | 945 | 803 |
2NO(g)+2CO(g)N2(g)+2CO2(g) ΔH
①ΔH=______________________________kJ·mol1。
②该反应的平衡常数与外界因素X(代表温度、压强、![]() 或催化剂接触面)关系如下图所示。
或催化剂接触面)关系如下图所示。
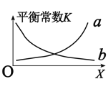
X是______,能正确表达平衡常数K随X变化的曲线是_______(填:a或b)。
⑶在一定温度和催化剂作用下,8NH3(g)+8NO(g)+2NO2(g)9N2(g)+12H2O(g)在2L密闭容器中通入4molNH3、4molNO、nmolNO2,经10分钟时达到平衡时,c(NH3)=0.5mol·L1,c(NO2)=0.25mol·L1。
①n=_____;
②υ(NO)=______;
③NH3的平衡转化率为_________。
⑷用电解法将某工业废水中CN-转变为N2,装置如下图所示。电解过程中,阴极区电解质溶液的pH将____________(填:增大、减小或不变)。阳极的电极反应式为______________。