题目内容
【题目】建设“美丽中国”首先要做好环境保护与治理。氮氧化物(NOx)是严重的大气污染物,其主要来源有汽车尾气和硝酸工厂等。氮氧化物(NOX)能引起雾霾、光化学烟雾、酸雨等环境问题。某科研机构设计了如下转化氮氧化物的几种方案。请回答下列问题:
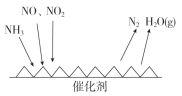
(1)方案Ⅰ:利用甲烷在催化剂条件下还原NOx,相关反应如下:
①N2(g)+O2(g)=2NO(g) H1=+180.5kJ/mol
②CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) H2=-574kJ/mol
③CH4(g)+4NO(g)=2N2(g)+ CO2(g)+2H2O(l) H3=-1160kJ/mol
则表示甲烷燃烧热的热化学反应方程式是 ___ 。
(2)方案Ⅱ:利用CO在催化剂条件下还原NOx:2NOx(g)+2CO(g)N2(g)+2CO2(g) H。向容积均为2L的甲(温度为T1)、乙(温度为T2)两个恒容密闭容器中分别充入2 mol NO2(g)和3 mol CO(g)。反应过程中两容器内CO2的物质的量浓度随时间的变化关系如图所示:
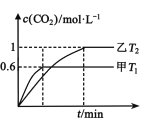
①甲容器中,平衡时NO2的转化率为____;
②T1___T2(填“>”或“<”);△H___0(填“>”或“<”),判定的依据是____;
③T2温度时,该反应的平衡常数K=____;
④乙容器达到平衡后,再充入3 mol NO2和2 molCO2,此时v(正)___v(逆)(填“>”“<”或“=”)。
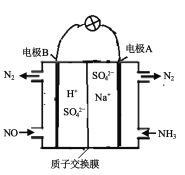
(3)方案3:可以利用原电池原理处理氮氧化合物,原理如图。则其正极的电极反应式为____。
【答案】CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=799kJ/mol ![]() > < 温度升高,c(CO2)低,平衡逆向移动,正反应为放热反应 16 = 2NO+4e-+4H+=N2+2H2O
> < 温度升高,c(CO2)低,平衡逆向移动,正反应为放热反应 16 = 2NO+4e-+4H+=N2+2H2O
【解析】
(1)甲烷完全燃烧的化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l),
根据①N2(g)+O2(g)=2NO(g) △H=+180.5kJmol1;
②CH4(g)+4NO2(g)=4NO(g)+4CO2(g)+2H2O(1) △H=574kJmol1;
③CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(1) △H=1160kJmol1;
根据盖斯定律①×2+③可得,CH4(g)+2O2(g)=CO2(g)+2H2O(l)的焓变△H=+180.5kJmol1×2+(1160kJmol1)=799kJ/mol,热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=799kJ/mol,
故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=799kJ/mol;
(2)①根据三段式:

则平衡时NO2的转化率为![]() ,故答案为:
,故答案为:![]() 。
。
②根据 分析可知,T1时先达到平衡,速率快,T1>T2,温度升高,c(CO2)低,平衡逆向移动,该反应的正反应为放热反应,故答案为:>;<;温度升高,c(CO2)低,平衡逆向移动,正反应为放热反应。
分析可知,T1时先达到平衡,速率快,T1>T2,温度升高,c(CO2)低,平衡逆向移动,该反应的正反应为放热反应,故答案为:>;<;温度升高,c(CO2)低,平衡逆向移动,正反应为放热反应。
③根据三段式:
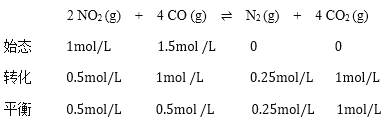
该反应的平衡常数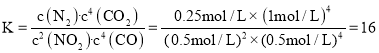 ,故答案为:16。
,故答案为:16。
④乙容器达到平衡后,再充入1.5mol/LNO2和1mol/LCO2,则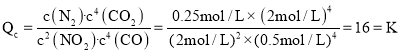 ,则反应仍是平衡状态,v(正)=v(逆),故答案为:=。
,则反应仍是平衡状态,v(正)=v(逆),故答案为:=。
(3)根据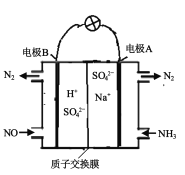 可知,电极A上发生氧化反应,为负极,电极B上发生还原反应,为正极,电解质溶液为酸性溶液,则正极的电极反应式为:2NO+4e-+4H+=N2+2H2O,故答案为:2NO+4e-+4H+=N2+2H2O。
可知,电极A上发生氧化反应,为负极,电极B上发生还原反应,为正极,电解质溶液为酸性溶液,则正极的电极反应式为:2NO+4e-+4H+=N2+2H2O,故答案为:2NO+4e-+4H+=N2+2H2O。

【题目】工业上常用绿柱石(主要成分3BeOAl2O36SiO2,还含有铁元素)冶炼铍,其简化的工艺流程如图所示:
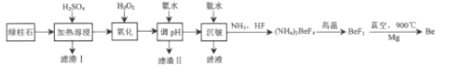
已知:Be和Al性质相似:几种金属阳离子的氢氧化物沉淀时的pH如表:
Be2+ | Al3+ | Fe3+ | Fe2+ | |
开始沉淀时 | 5.2 | 3.3 | 1.5 | 6.5 |
沉淀完全时 | 8.8 | 5.0 | 3.7 | 9.7 |
回答下列问题:
(1)滤渣Ⅰ的主要成分是______,加入H2O2的作用是______。
(2)得到滤渣Ⅱ的合理pH范围是______。
(3)用化学方程式解释不宜使用NaOH溶液来沉铍的原因是______。
(4)得到(NH4)2BeF4的化学方程式为______。
(5)由Mg还原BeF2得到Be需要真空的环境,其原因是______。
(6)若绿柱石中BeO的含量为a%,1吨绿柱石能生产含铍2%的合金b吨,则Be的利用率为______。(用含a、b的表达式表示)