题目内容
【题目】HCHO与O2在羟基磷灰石(HAP)表面反应通过两步反应生成CO2、H2O的机理如图所示(图中只给出了HAP的部分结构)。下列说法错误的是( )
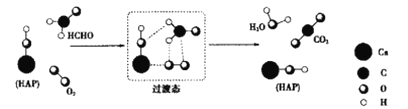
A.HCHO在反应过程中,所有C-H键都发生断裂
B.反应第一步是吸热过程
C.产物H2O中的O全部来自于O2
D.HAP是该反应的催化剂
【答案】BC
【解析】
A.HCHO在反应中有C-H断裂和C=O键形成,所以甲醛被氧化生成二氧化碳和水,故A正确;
B.断键吸收能量、成键放出能量,第一步没有化学键断裂,所以不需要吸收热量,故B错误;
C.产物中的水中的O部分来自于氧气,故C错误;
D.第一步反应中作反应物、第二步反应中作生成物,所以HAP是该反应的催化剂,故D正确;
答案选BC。

练习册系列答案
相关题目