题目内容
【题目】Ⅰ.回答下列问题:
(1)烃A的结构简式为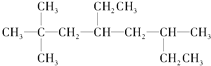 ,用系统命名法命名烃A:____________。
,用系统命名法命名烃A:____________。
(2)某烃的分子式为![]() ,核磁共振氢谱图中显示4个峰,则该烃的一氯代物有_______种,该烃的结构简式为____________。
,核磁共振氢谱图中显示4个峰,则该烃的一氯代物有_______种,该烃的结构简式为____________。
(3)麻黄素又称黄碱,是我国特定中药材麻黄中所含有的一种生物碱。经科学家研究发现其结构为: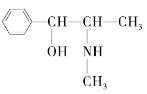 ,下列各物质:A.
,下列各物质:A. 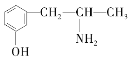 B.
B. ![]() C.
C. 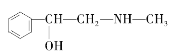 D.
D. 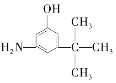 E.
E. 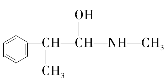
与麻黄素互为同分异构体的是_________(填字母,下同),互为同系物的是___________(填字母)。
Ⅱ.有机物C常用于食品行业。已知![]() 在足量
在足量![]() 中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重
中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重![]() 和
和![]() ,经检验剩余气体为
,经检验剩余气体为![]() 。
。
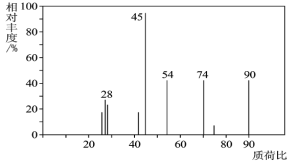
(1)C分子的质谱图如图所示,从图中可知其相对分子质量是________,则C的分子式是_______。
(2)C能与![]() 溶液发生反应,C一定含有的官能团是_____________。
溶液发生反应,C一定含有的官能团是_____________。
(3)C分子的核磁共振氢谱有4个峰,峰面积之比是![]() ,则C的结构简式是________。
,则C的结构简式是________。
(4)![]() 与
与![]() 的氢氧化钠溶液反应,需溶液的体积是_____
的氢氧化钠溶液反应,需溶液的体积是_____![]() 。
。
【答案】2,2,6-三甲基-4-乙基辛烷 4 ![]() DE C 90
DE C 90 ![]() 羧基或
羧基或![]()
![]() 100
100
【解析】
Ⅰ.(1)根据烷烃的命名原则命名;
(2)核磁共振氢谱图中显示4个峰,说明结构存在四种氢原子,据此分析解答;
(3)根据同分异构体和同系物的概念分析判断;
Ⅱ.根据最大质荷比可确定相对分子质量为90,根据生成的水和二氧化碳的计算含有的H和C的物质的量及质量,判断有机物中含有O元素的质量,再根据n(C)∶n(H)∶n(O)确定C的实验式和化学式,据此分析解答。
Ⅰ.(1) 为烷烃,最长碳链含有8个C,主链为辛烷,编号从距离甲基最近的一端开始,在2号C和6号C上各含有2个、1个甲基,在4号C含有1个乙基,该有机物名称为:2,2,6-三甲基-4-乙基辛烷,故答案为:2,2,6-三甲基-4-乙基辛烷;
为烷烃,最长碳链含有8个C,主链为辛烷,编号从距离甲基最近的一端开始,在2号C和6号C上各含有2个、1个甲基,在4号C含有1个乙基,该有机物名称为:2,2,6-三甲基-4-乙基辛烷,故答案为:2,2,6-三甲基-4-乙基辛烷;
(2)某烃的分子式为![]() ,核磁共振氢谱图中显示4个峰,为异戊烷,分子中含四种氢原子,生成的一氯代物四种,该烃结构简式为:CH3CH(CH3)CH2CH3,故答案为:4;CH3CH(CH3)CH2CH3;
,核磁共振氢谱图中显示4个峰,为异戊烷,分子中含四种氢原子,生成的一氯代物四种,该烃结构简式为:CH3CH(CH3)CH2CH3,故答案为:4;CH3CH(CH3)CH2CH3;
(3)分子式相同而结构不同的有机物互称同分异构体,题中D、E与麻黄素分子式相同,而结构不同,互为同分异构体,其中C与麻黄素的结构相似,分子组成上相差1个CH2原子团,互为同系物,故答案为:DE;C;
Ⅱ.(1)由图中最大质荷比可确定相对分子质量为90,5.4g水的物质的量为![]() =0.3mol,n(H)=0.6 mol,13.2g二氧化碳的物质的量为
=0.3mol,n(H)=0.6 mol,13.2g二氧化碳的物质的量为![]() =0.3mol,n(C)=n(CO2)=0.3 mol,此有机物9.0g含O元素质量为9.0g-0.6g-0.3×12 g=4.8 g,n(O)=
=0.3mol,n(C)=n(CO2)=0.3 mol,此有机物9.0g含O元素质量为9.0g-0.6g-0.3×12 g=4.8 g,n(O)=![]() =0.3 mol,故n(C)∶n(H)∶n(O)=0.3mol∶0.6mol∶0.3mol=1∶2∶1,因此实验式为CH2O,设分子式为(CH2O)n,A的相对分子质量为90,可得30n=90,解得:n=3,故有机物A为C3H6O3,故答案为:90;C3H6O3;
=0.3 mol,故n(C)∶n(H)∶n(O)=0.3mol∶0.6mol∶0.3mol=1∶2∶1,因此实验式为CH2O,设分子式为(CH2O)n,A的相对分子质量为90,可得30n=90,解得:n=3,故有机物A为C3H6O3,故答案为:90;C3H6O3;
(2)C能与NaHCO3溶液发生反应,说明C中含有羧基(-COOH),故答案为:羧基或-COOH;
(3)有机物C的分子式为C3H6O3,核磁共振氢谱有4个峰,峰面积之比是1∶1∶1∶3,则分子中4种H原子的数目为1、1、1、3,分子中含有1个-COOH、1个-CH3、1个![]() 、1个-OH,有机物C的结构简式为
、1个-OH,有机物C的结构简式为![]() ,故答案为:
,故答案为:![]() ;
;
(4)有机物C含有1个-OH和1个-COOH,只有-COOH能够与NaOH反应,0.1molC消耗0.1molNaOH,需要1.0mol/L的氢氧化钠溶液的体积为![]() =0.1L=100mL,故答案为:100。
=0.1L=100mL,故答案为:100。

 字词句段篇系列答案
字词句段篇系列答案【题目】一定温度下,在三个体积均为2.0 L的恒容密闭容器中发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)。
PCl3(g)+Cl2(g)。
编号 | 温度 /℃ | 起始物质 的量/mol | 平衡物质 的量/mol | 达到平衡 所需时间/s | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t |
Ⅱ | 320 | 0.80 | t1 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t2 |
下列说法正确的是
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
C.反应到达平衡时,容器Ⅰ中的平均速率为v(PCl5)=![]() mol·L-1·s-1
mol·L-1·s-1
D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl3 0.45 mol和Cl2 0.10 mol,则反应将向逆反应方向进行
【题目】1799年由英国化学家汉弗莱·戴维发现一氧化二氮(N2O)气体具有轻微的麻醉作用,而且对心脏、肺等器官无伤害,后被广泛应用于医学手术中。
(1)一氧化二氮早期被用于牙科手术的麻醉,它可由硝酸铵在催化剂下分解制得,该反应的化学方程式为___。
(2)已知反应2N2O(g)=2N2(g)+O2(g) ΔH=-163kJ·mol-1,1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收945kJ、498kJ的能量,则1molN2O(g)分子中化学键断裂时需要吸收的能量为___kJ。
(3)一定温度下的恒容容器中,反应2N2O(g)=2N2(g)+O2(g)的部分实验数据如下:
反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
c(N2O)/mol·L-1 | 0.10 | 0.09 | 0.08 | 0.07 | 0.06 | 0.05 | 0.04 | 0.03 | 0.02 | 0.01 | 0.00 |
①在0~20min时段,反应速率v(N2O)为___mol·(L·min)-1。
②若N2O起始浓度c0为0.150mol·L-1,则反应至30min时N2O的转化率α=___。
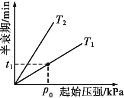
③不同温度(T)下,N2O分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度N2O消耗一半时所需的相应时间),则T1___(填“>”“=”或“<”)T2。当温度为T1、起始压强为p0时,反应至t1min时,体系压强p=___(用p0表示)。
(4)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步 I2(g)=2I(g)(快反应)
第二步 I(g)+N2O(g)![]() N2(g)+IO(g)(慢反应)
N2(g)+IO(g)(慢反应)
第三步 IO(g)+N2O(g)![]() N2(g)+O2(g)+I(g)(快反应)
N2(g)+O2(g)+I(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是___(填标号)。
A.温度升高,k值增大
B.第一步对总反应速率起决定作用
C.第二步活化能比第三步大
D.I2的浓度与N2O分解速率无关