题目内容
【题目】 根据相应的图象(图象编号与答案一一对应),判断下列相关说法正确的是( )
A.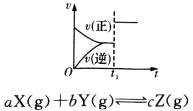 B.
B.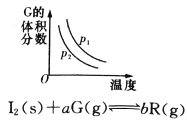
C.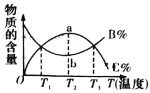 D.
D.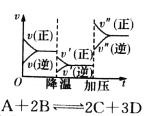
A.t0时改变某一条件有如图所示,则改变的条件一定是加入催化剂
B.反应达到平衡时,外界条件对平衡影响关系如图所示,则正反应为放热反应
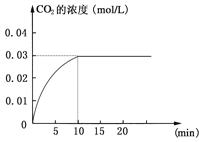
C.从加入反应物开始,物质的百分含量与温度关系如图所示,则该反应的正反应为吸热反应
D.反应速率和反应条件变化如图所示,则该反应正反应为放热反应,A、B、C是气体、D为固体或液体
【答案】C
【解析】
试题分析:A.若a+b=c,改变的条件可能为增大压强,则不一定为催化剂,故A错误;
B、图象分析可知,升温,G的体积分数减小,说明平衡正向移动,正向是吸热反应,不是放热反应,故B错误;C.由图可知,反应从正向开始,B为反应物,T2为平衡状态,升高温度,B的含量增大,平衡向逆反应方向移动,则正反应为放热反应,故C正确;D.降温,正反应速率大,平衡向正反应方向移动,正反应为放热反应;加压,正反应速率大,平衡向正反应方向移动,则正反应方向是气体体积减小的分析,A、B、C是气体、D为固体或液体,或者A、B中至少有一种是气体,C、D为固体或液体,故D错误;故选C。

 高中必刷题系列答案
高中必刷题系列答案【题目】4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。
m | n | ||
x | y |
回答下列问题:
(1)元素x在周期表中的位置是 ,其单质可采用电解熔融 的方法制备。
(2)气体分子(mn)2的电子式为 ,(mn)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为 。
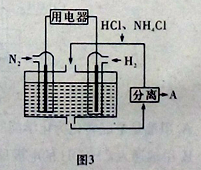
(3)已知氰化钠(NaCN),可以与很多金属形成络合物,因此工业上采用氰化法提炼金:用稀的氰化钠溶液处理粉碎了的金矿石,通入空气,使金矿石中的金粒溶解,生成能溶于水的络合物Na[Au(CN)2],其反应方程式为:①4Au+8NaCN+2H2O+O2=4Na[Au(CN)2]+4NaOH,Na[Au(CN)2]在水溶液中的电离方程式为:②Na[Au(CN)2]=Na++[Au(CN)2]-,然后再用锌从溶液中把金置换出来,锌转化为Na2[Zn(CN)4]。据此,请利用①写出在空气中用氰化钠溶液提取金的电极反应式:正极: ,负极: 。
(4)若人不慎氰化钠中毒,可用Na2S2O3缓解,二者反应得到两种含硫元素的离子,其中一种遇到Fe3+可变为红色。写出解毒原理的相关离子方程式 。