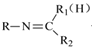
题目内容
【题目】甲醇是重要的化工原料,也可作燃料。工业上可用CO2和H2在一定条件下合成甲醇。回答下列问题。
(1)已知:CO 和 H2 的燃烧热分别为 283.0 kJ·mol-1、285.8kJ·mol-1 ,水的汽化热为 44.0kJ·mol-1, 反应① CO+H2O=CO2+H2 是生成合成甲醇的原料气(CO2、H2)的重要反应,其热化学方程式为: CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =_____ kJ·mol-1。
(2)某同学设计实验对反应①进行研究。将 1mol H2O(g)和 1mol CO 充入一个恒容密闭容器中,在催化剂和一定温度下达到化学平衡。如图是 CO 的平衡转化率(%)随温度变化的曲线,260℃时反应①的平衡常数 K=_______。
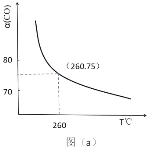
(3)CO2和 H2在催化剂、一定温度下合成甲醇。图为在容积为 1L 的恒容密闭容器中,加入 3 molH2和 1molCO2时经过相同时间甲醇产率与反应温度的关系曲线:
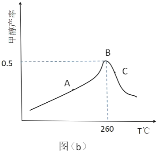
曲线上 A 点_____(填“是”或“不是”)对应温度下的平衡产率,理由是_____,C 点甲醇的产率低于 B 点的原因可能是_____(填标号)。
A.反应活化能增大 B.催化剂活性低 C.副反应多 D.平衡常数变大 E.平衡逆向移动
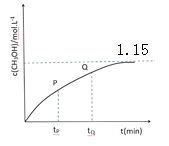
(4)CO和 H2在一定条件下也可以合成甲醇。在容积为1L的恒容密闭容器中,加入 a molH2和2.0molCO,在催化剂和 260℃温度条件下发生反应:CO+2H2=CH3OH。图为甲醇的浓度与反应时间的关系曲线,tP 时的 v 逆_____tQ 时的 v 逆(填大于、小于或等于),判断的依据是_____,达平衡时氢气的浓度为 1.0mol/L,则起始时加入的氢气的物质的量为_____mol。
【答案】-41.2 9 不是 该反应为放热反应,平衡产率随温度的升高而降低 BCE 小于 tP 时的甲醇浓度小于tQ 时浓度,反应速率更慢 3.3
【解析】
(1)H2的燃烧热为-285.8kJ·mol-1,故热化学方程式为H2(g)+![]() O2(g)=H2O(l)△H=-285.8KJ·mol-1;CO的燃烧热为-283.0kJ·mol-1,故热化学方程式为①CO(g)+
O2(g)=H2O(l)△H=-285.8KJ·mol-1;CO的燃烧热为-283.0kJ·mol-1,故热化学方程式为①CO(g)+![]() O2(g)=CO2(g)△H=-283.0KJ·mol-1,②H2(g)+O2(g)=H2O(l)△H=-285.8KJ·mol-1,③H2O(l)=H2O(g)△H=+44.0KJ·mol-1,1×①-②-③得, CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =-41.2kJ·mol-1。故答案为:-41.2;
O2(g)=CO2(g)△H=-283.0KJ·mol-1,②H2(g)+O2(g)=H2O(l)△H=-285.8KJ·mol-1,③H2O(l)=H2O(g)△H=+44.0KJ·mol-1,1×①-②-③得, CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =-41.2kJ·mol-1。故答案为:-41.2;
(2)对反应①CO(g)+H2O(g)=CO2(g)+H2(g) 进行研究。

260℃时反应①的平衡常数 K=![]() =9。故答案为:9;
=9。故答案为:9;
(3)曲线上 A 点不是对应温度下的平衡产率,理由是该反应为放热反应,平衡产率随温度的升高而降低,C 点甲醇的产率低于 B 点的原因可能是:A.反应活化能增大,不影响产率,故错误; B.催化剂活性低,产率降低,故正确; C.副反应多,消耗大量原料,故正确; D.平衡常数变大,平衡正向移动,产率升高,故错误;E.平衡逆向移动,产率降低,故正确;故选BCE;故答案为:不是;该反应为放热反应,平衡产率随温度的升高而降低;BCE;
(4)甲醇的浓度与反应时间的关系曲线可知,tP 时的 v 逆小于tQ 时的 v 逆,tP 时的甲醇浓度小于tQ 时浓度,反应速率更慢;由图平衡时c(CH3OH)= 1.15mol·L-1,由方程式CO+2H2=CH3OH得氢气的浓度变化量为2.3mol·L-1,起始时加入的氢气的浓度为(2.3+1)mol·L-1=3.3mol·L-1,则起始时加入的氢气的物质的量为3.3mol;故答案为:小于:tP 时的甲醇浓度小于tQ 时浓度,反应速率更慢;3.3。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案【题目】NiCl2是化工合成中最重要的镍源,在实验室中模拟工业上以金属镍废料(含Fe、Al等杂质)为原料生产NiCl2的工艺流程如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Ni(OH)2 |
开始沉淀的pH | 2.1 | 6.5 | 3.7 | 7.1 |
沉淀完全的pH | 3.3 | 9.7 | 4.7 | 9.2 |
(1)为了提高镍元素的浸出率,在“酸浸”时可采取的措施有__________(写一条即可)。
(2)加入H2O2时发生主要反应的离子方程式为__________。
(3)“调pH”时,控制溶液pH的范围为__________。
(4)“沉镍”过程中,若滤液A中c(Ni2+)=1.0mol/L,欲使100mL该滤液中的Ni2+沉淀完全[即溶液中c(Ni2+)≤1.0×10-5],则需用托盘天平称取Na2CO3固体的质量至少为_____g。(已知Ksp(NiCO3)=6.5×10-6,忽略溶液体积的变化)
(5)流程中由溶液得到NiCl2·6H2O的实验操作步骤依次为______、过滤、洗涤、干燥。