题目内容
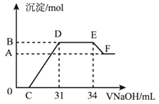
【题目】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铁铝合金与很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液x中,逐滴加入4molL﹣1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。则下列有关计算和判断正确的是( )
A.溶液x中所含的阳离子有:Al3+、H+、Fe3+、Fe2+
B.在DE段,发生反应的离子方程式为NH4++OH﹣→NH3H2O
C.无法求出B点对应的沉淀的物质的量
D.C点对应的氢氧化钠溶液的体积为7mL
【答案】BD
【解析】
铝粉和铁粉的混合物与一定量很稀HNO3充分反应,被氧化为Al3+、Fe3+,通过题意,反应始终没有气体生成,可以得出不会有氮的氧化物生成,又有硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,可以推测N元素由+5变成了﹣3价,由图可得硝酸过量,加入氢氧化钠溶液应先与硝酸反应,再生成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可得与NH4+发生了反应,则随着NaOH的滴加,发生的反应依次有:
①H++OH﹣=H2O,
②Fe3++3OH﹣=Fe(OH)3↓,Al3++3OH﹣=Al(OH)3↓,
③NH4++OH﹣═NH3H2O,
④Al(OH)3+OH﹣=AlO2﹣+2H2O,据此分析解答。
A.根据图示得到的溶液和氢氧化钠反应产生沉淀的情况可以知道,金属铁和稀硝酸反应生成硝酸铁、硝酸铵和水,反应的离子方程式为:8Fe+30H++3NO3﹣=8Fe3++3NH4++9H2O,金属铝和硝酸反应生成硝酸铝、硝酸铵和水,溶液x中所含的阳离子有:Al3+、H+、Fe3+、NH4+,硝酸过量,不可能生成亚铁离子,故A错误;
B.DE一段沉淀的量没有发生变化,为NH4NO3和NaOH反应,反应的离子方程式为NH4++OH﹣═NH3H2O,故B正确;
C.图中OC段没有沉淀生成,此阶段发生的离子方程式为H++OH﹣=H2O;在DE段沉淀的物质的量没有变化,应为NH4+和OH﹣的反应,此阶段发生反应的离子方程式为NH4++OH﹣═NH3H2O;根据NH4++OH﹣═NH3H2O 得:n(NH4+)=(34﹣31)×10﹣3L×4mol/L=0.012 mol,根据氧化还原反应,N元素由+5价变为﹣3价,而金属都由0价变为+3价,可以运用电子守恒得出金属的物质的量为:![]() =0.032mol,所以生成沉淀的物质的量为0.032mol,故C错误;
=0.032mol,所以生成沉淀的物质的量为0.032mol,故C错误;
D.金属的物质的量为0.032mol,根据金属离子带3个正电荷分析,铝离子和铁离子生成沉淀需要的氢氧化钠的体积为![]() L=24mL,则C点氢氧化钠溶液的体积为31mL﹣24mL=7mL,故D正确;
L=24mL,则C点氢氧化钠溶液的体积为31mL﹣24mL=7mL,故D正确;
故选:BD。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案【题目】用下图所示装置分别进行下列实验:将①中溶液滴入②中,按要求填写下列空格:

方案 | ①中物质 | ②中物质 | 填空编号及要求 |
实验1 | 滴加过酚酞的水 | Na2O2 | 写出会看到的现象①_____ |
实验2 | NaOH溶液 | 未打磨过的铝条 | 写出所发生反应的离子方程式 ②_____ |
实验3 | 盐酸 | NaAlO2溶液 | 画出生成沉淀量随盐酸的加入的变化图象 ③_____ |
实验4 | 稀盐酸 | Na2CO3与NaOH的混合溶液 | 已知生成气体量随盐酸的加入的变化图象如下,则原溶液中的Na2CO3与NaOH的物质的量浓度之比为 ④_____
|
实验5 | FeCl3和盐酸的混合液 | 等质量的铜、锌、铁三种金属的混合物 | 若反应后无固体剩余,则反应后的溶液中一定存在的阳离子是 ⑤_____ |