题目内容
1.同温同压下,若A容器中充满气体Ox和B容器中充满气体Oy(1)若所含分子总数相等,则A容器和B容器的容积之比是1:1(用x、y表示,下同)
(2)若两容器中所含原子总数相等,则A容器和B容器的容积比是y:x
(3)若两容器的体积比为y:x,则Ox和Oy物质的量之比为y:x,质量之比为1:1,密度之比为x:y.
分析 (1)同温同压下,根据n=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$计算;
(2)根据分子的组成判断气体物质的量的关系,根据n=$\frac{V}{{V}_{m}}$计算;
(3)根据n=$\frac{V}{{V}_{m}}$计算物质的量,根据m=nM计算质量之比,两种气体的密度之比是相应的摩尔质量之比.
解答 解:(1)同温同压下,气体的Vm相等,根据n=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$计可知:气体的分子数之比等于气体的体积之比,故答案为:1:1;
(2)若A容器中充满气体Ox和B容器中充满气体Oy,两容器中所含原子总数相等,则根据分子组成可知,两容器中的分子数之比等于y:x,可知:气体的分子数之比等于气体的体积之比,为y:x,
故答案为:y:x2;
(3)若两容器的体积比为y:x,根据n=$\frac{V}{{V}_{m}}$可知Ox和Oy物质的量之比为y:x,质量之比等于y×16x:x×16y=1:1,所以质量之比为1:1,密度之比等于摩尔质量之比为16x:16y=x:y;
故答案为:y:x;1:1;x:y.
点评 本题考查阿伏加德罗定律及推论的应用,题目难度中等,注意物质的量的有关计算公式的运用,侧重于考查学生的计算能力和分析能力.

练习册系列答案
相关题目
9.同温同压下,三个等体积的干燥圆底烧瓶中分别充满①HCl ②NO2③体积比为1:1的NO2和O2,进行喷泉实验.经充分反应后烧瓶内溶质的物质的量浓度之比为( )
| A. | 1:1:1 | B. | 4:4:5 | C. | 5:5:4 | D. | 15:10:12 |
16.在其他条件不变时,某气体的体积与温度(K)成正比.在不同温度时有的气体还会形成不同分子数的缔合物.一下是该气态物质在不同温度时测得的密度.
今测得1600K时该物质的分子组成为AB2,则在其余温度时它的化学式应分别为(800K)时:AB2(400K)时:A2B4(200K)时:A4B8.
| 温度/K | 200 | 400 | 800 | 1600 |
| 密度/g•cm-3 | 3.21 | 0.81 | 0.20 | 0.11 |
13.已知甲醛与乙酸完全燃烧的热化学方程式如下所示:
①HCHO(g)+O2(g)→CO2(g)+H2O(l)+571kJ
②CH2COOH(g)+2O2(g)→2CO2(g)+2H2O(l)+926kJ
下列说法正确的是( )
①HCHO(g)+O2(g)→CO2(g)+H2O(l)+571kJ
②CH2COOH(g)+2O2(g)→2CO2(g)+2H2O(l)+926kJ
下列说法正确的是( )
| A. | 1mol HCHO(g)完全燃烧生成气态水时放热大于571kJ | |
| B. | 1mol CH3COOH(l)完全燃烧生成液态水时放热大于926kJ | |
| C. | 相同条件下,等质量的HCHO(g)与CH3COOH(g)所含能量相比,前者更高 | |
| D. | 相同条件下,等质量的HCHO(g)与CH3COOH(g)完全燃烧,后者放热更多 |
3.下列说法中正确的是( )
| A. | 油脂的水解即皂化反应 | |
| B. | 油脂中液态的是纯净物,固态的是混合物 | |
| C. | 因为油脂的相对分子质量都很大,所以它们都比水重 | |
| D. | 油脂属于高级脂肪酸甘油酯 |
 ,第一电离能最小的元素是Cu(填元素符号).
,第一电离能最小的元素是Cu(填元素符号).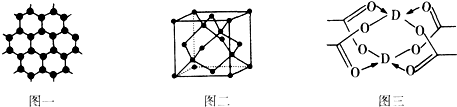
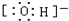 .
.