题目内容
12.现有容积为1L的恒温恒容密闭容器,向其中加入2mol A气体和2mol B气体后发生如下反应:A(g)+B(g)═C(g)△H=-a kJ•mol-1,20s后,反应达到平衡状态,生成1mol C气体,放出热量Q1kJ.回答下列问题.
①计算20s内B气体的平均化学反应速率为0.05mol/(L•s).
②保持容器温度和容积不变,若改为向其中加入1molC气体,反应达到平衡时,吸收热量Q2kJ,则Q1与Q2的相互关系正确的是C(填字母).
(A)Q1+Q2=a (B) Q1+2Q2<2a (C)Q1+2Q2>2a (D)Q1+Q2<a
③在原平衡基础上,保持容器温度和容积不变,向容器中再通入bmolA气体(b>0)时,v(正)>v(逆)(填“>”、“<”或“=”),重新达平衡后,C气体的平衡体积分数φ(C)=$\frac{1}{3}$,则b=1.33.
分析 ①根据反应速率v=$\frac{△c}{△t}$计算;
②加入1molA气体和1molB气体与加入1molC气体是在保持恒温、恒容情况下是等效平衡,加入2molA气体和2molB气体与加入1molA气体和1molB气体相比,相当于增大一倍的压强,增大压强,反应向体积缩小的方向正向移动;
③增加反应物的浓度平衡向正反应方向移动,由题意2molA气体和2molB气体生成1molC气体,根据三段式求得平衡常数K=1,依据温度不变,平衡常数不变进行解答.
解答 解:①容积为1L的恒温恒容密闭容器,20s内生成1molC气体,根据A(g)+B(g)?C(g)△H=-a kJ•mol-1,B气体减少1mol,浓度减少1.0 mol/L,c(B)=1.0mol/L,△t=20s,v=$\frac{△c}{△t}$=$\frac{1.0mol/L}{20s}$=0.05mol/(L•s);
故答案为:0.05mol/(L•s);
②设加入1molA气体和1molB气体达到平衡时,放出的热量为Q3,根据等效平衡可知:保持容器温度和容积不变,加入1molA气体和1molB气体与加入1molC气体是等效的,则Q2+Q3=a=Q1,又知保持容器温度和容积不变,加入2molA气体和2molB气体与加入1molA气体和1molB气体相比,相当于增大一倍的压强,A(g)+B(g)?C(g)从起始量分析,正反应是体积缩小的反应,增大压强,反应向体积缩小的方向移动,所以平衡正向移动,所以放出的热量Q1>2Q3,所以Q1 +2Q2>2a,所以选:C;
故答案为:C;
③在原平衡基础上,保持容器温度和容积不变,向容器中再通入bmolA气体(b>0)时,平衡正向移动,则v(正)> v(逆),由题意2molA气体和2molB气体生成1molC气体,根据三段式:
A(g)+B(g)=C(g)
开始(mol/L) 2 2 0
反应(mol/L) 1 1 1
平衡(mol/L) 1 1 1
平衡常数K=$\frac{c(C)}{c(A)c(B)}$=$\frac{1}{1×1}$=1,再通入bmolA气体,温度不变,平衡常数不变,根据三段式:
A(g)+B(g)=C(g)
开始(mol/L) 2+b 2 0
反应(mol/L) x x x
平衡(mol/L)2+b-x 2-x x
又知K=1,ϕ(C)=$\frac{1}{3}$,所以$\frac{x}{(2+b-x)(2-x)}$=1,$\frac{x}{4+b-x}$=$\frac{1}{3}$,解得b=1.33,x=1.33;
故答案为:>;1.33.
点评 本题主要考查平衡的有关知识,掌握化学平衡常数的计算方法,以及化学平衡移动原理知识的灵活运用是解答的关键,题目难度较大,注意三段式的运用.

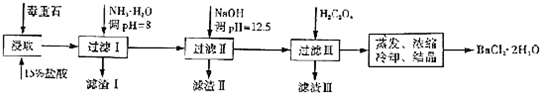
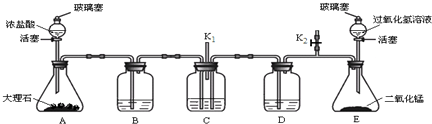
(1)毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而使反应速率加快.实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的ac.
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行.
已知:2CrO42-+2H+═Cr2O72-+H2O Ba2++CrO42-═BaCrO4↓
步骤Ⅰ移取xml一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL.
步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL.则BaCl2溶液的浓度为$\frac{({V}_{0}-{V}_{1})b}{y}$mol•L-1.
| A. | 钢化玻璃 | B. | 光学玻璃 | C. | 石英玻璃 | D. | 有色玻璃 |
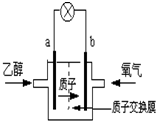 2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺 酸类质子溶剂,在200°C左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意如图,下列说法不正确的是( )
2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺 酸类质子溶剂,在200°C左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意如图,下列说法不正确的是( )| A. | a极为电池的负极 | |
| B. | 电池工作时电流由b极沿导线经灯泡再到a极 | |
| C. | 电池工作时,1mol乙醇被还原时就有6mol电子转移 | |
| D. | 电池正极的电极反应为:4H++O2+4e-→2H2O |
| A. | 某地燃烧化石燃料排放的废气中含CO2、SO2,使雨水pH=6形成酸雨 | |
| B. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| C. | 高空臭氧层吸收太阳紫外线,保护地球生物;反应3O2=2O3有单质参加,属于氧化还原反应 | |
| D. | 人造纤维,合成纤维和光导纤维都是有机高分子化合物 |
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH$→_{170℃}^{H_{2}So_{4}(浓)}$CH2=CH2+H2O,CH2=CH2+Br2→BRCH2B
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚;浓硫酸把乙醇氧化为CO2等.
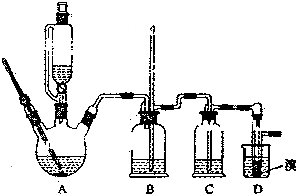
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下;
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/°C | 78.5 | 132 | 34.6 |
| 熔点/°C | -130 | 9 | -116 |
(1)A装置上方使用滴液漏斗的优点是:便于漏斗内液体顺利流下;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(2)B装置的作用是平衡压强,检查装置是否发生堵塞.
(3)在装置C中应加入C(填正确选项前的字母),其目的是吸收反应产物的SO2和CO2酸性气体.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去.
(5)D装置具支试管内若用嗅水代替液溴(假定产物相同),分析其优点生成的1,2-二溴乙烷和水分层,水在上层起液封作用,防止产品挥发.
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.