题目内容
【题目】下列解释事实的方程式不正确的是( )
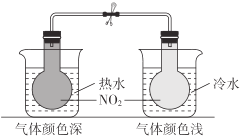
A.将装有NO2的玻璃球浸入热水中颜色加深:2NO2(g)![]() N2O4(g) ΔH>0
N2O4(g) ΔH>0
B.用Na2S处理含Hg2+废水:Hg2++S2-=HgS↓
C.Na2S2O3溶液与稀H2SO4混合产生浑浊:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O
D.闪锌矿(ZnS)经CuSO4溶液作用转变为铜蓝(CuS):ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq)
【答案】A
【解析】
A.装有NO2的玻璃球浸入热水中颜色加深,说明NO2的浓度增大,反应2NO2(g)![]() N2O4(g)的平衡逆向移动;说明升高温度,平衡逆向移动,逆反应是吸热反应,正反应是放热反应,△H<0,A错误,符合题意;
N2O4(g)的平衡逆向移动;说明升高温度,平衡逆向移动,逆反应是吸热反应,正反应是放热反应,△H<0,A错误,符合题意;
B.利用Na2S处理含有Hg2+废水,由于HgS难溶于水,离子方程式为Hg2++S2-=HgS↓,B正确,不选;
C.Na2S2O3和酸反应可生成S和SO2,化学方程式为Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,C正确,不选;
D.CuS比ZnS难溶,因此闪锌矿(ZnS)经CuSO4溶液作用后,ZnS可以转化为更难溶的CuS,离子方程式为ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq),D正确,不选;
答案选A。

练习册系列答案
相关题目
【题目】根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
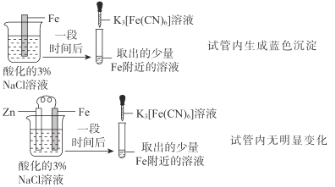
A |
| Zn保护了Fe不被腐蚀 |
B |
| 2NO2(g)N2O4(g)为吸热反应 |
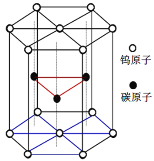
C |
| 木炭与浓硝酸发生了反应 |
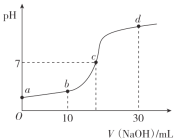
D |
| 碳酸钠的水解程度强 |
A.AB.BC.CD.D