题目内容
【题目】根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A |
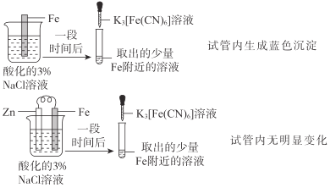
| Zn保护了Fe不被腐蚀 |
B |
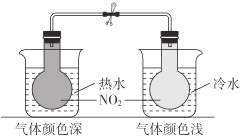
| 2NO2(g)N2O4(g)为吸热反应 |
C |
| 木炭与浓硝酸发生了反应 |
D |
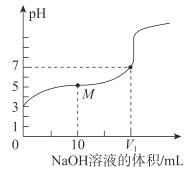
| 碳酸钠的水解程度强 |
A.AB.BC.CD.D
【答案】A
【解析】
A.只有Fe的实验中,加入K3[Fe(CN)6],得到蓝色沉淀,说明Fe被腐蚀,生成了Fe2+;Zn-Fe原电池的实验中,取Fe电极附近的溶液,加入K3[Fe(CN)6],没有得到蓝色沉淀,说明Fe没有被腐蚀,Zn保护了Fe不被腐蚀,故A正确;
B.热水中颜色深,可知升高温度,2NO2(g)N2O4(g)逆向移动,则正反应为放热反应,故B错误;
C.浓硝酸受热也可分解生成二氧化氮,不能说明木炭与浓硝酸发生了反应,故C错误;
D.比较两种离子的水解程度,需要使用相同离子浓度的溶液;室温下,碳酸钠的溶解性比碳酸氢钠大,则二者的饱和溶液中,两种物质的浓度不同,对应的阴离子浓度也不相同,因此本实验不合理,故D错误;
答案选A。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】某同学研究金属锌与氯化铜溶液之间反应,在实验中该同学观察到的现象有:
i.产生少量气泡;ii.有红色固体生成;iii.溶液中产生白色沉淀。
为了解释上述现象,某同学查阅资料,获得如下信息:
编号 | 化学反应离子方程式 |
1 | Zn+Cu2+ |
2 | Zn+2Cu2+ |
3 | Cu++2Cl- |
4 | Cu++Cl- |
(1)请结合离子方程式解释产生少量气泡的原因:___。
(2)Zn与CuCl2反应生成白色沉淀的离子方程式是___。
(3)为了探究影响生成白色沉淀的因素,该同学进一步实验。取不同浓度CuCl2溶液,加入锌并振荡,均立刻产生少量气泡和红色固体,其他实验现象如下。
| 编号 | 浓度(rnol/L) | 试剂(锌均过量) | 实验现象 |
a | 0.5 | 锌片 | 立刻出现少量白色沉淀 | |
b | 1 | 锌片 | 立刻出现白色沉淀 | |
1 | 锌粉 | 立刻出现大量白色沉淀 | ||
d | 1 | 锌片、适量NaCl固体 | 少量白色沉淀,振荡迅速溶解 |
①对比实验a、b,实验结论是___。
②某同学从化学平衡的角度分析,d中白色沉淀溶解可能的原因是___(用离子方程式表示)。为证明该同学分析的原因正确,向b试管中加入适量___,振荡,观察到___,证明该同学分析的原因正确。
(4)利用沉淀法除去杂质在实际生产中应用广泛。
①在工业中冶炼锌,为了除去ZnSO4电解液溶液中的C1-,可加入___和___,生成沉淀而除去。
②通过进一步查阅资料得知:CuCl的形成与溶液的pH及Cu2+等离子浓度有关,一定条件下,通过实验得出pH、Cu2+浓度对Cl-沉淀的影响如图所示:

根据图,除去该电解液中Cl-的最佳条件是___。