题目内容
7.已知两分子乙醛可发生下列反应:CH3CHO+CH3CHO→CH3-CH=CHCHO,则乙醛与丙醛的混合物发生上述加成反应的产物有 ( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
分析 乙醛与丙醛的混合物发生该加成反应的情况有:①两分子乙醛之间,②两分子丙醛之间,③乙醛和丙醛分子之间,其中①②各有一种产物,③中有两种产物,据此进行解答.
解答 解:乙醛与丙醛的混合物发生该加成反应的情况有:①两分子乙醛之间,②两分子丙醛之间,③乙醛和丙醛分子之间,
其中①的产物为:CH3-CH=CHCHO;
②的产物为:CH3CH2CH=C(CH3)CHO;
③的产物有两种:乙醛保留醛基时的产物为:CH3CH2CH=CHCHO;丙醛保留醛基时产物为:CH3CH=C(CH3)CHO,
所以总共有4种产物,
故选C.
点评 本题考查了加成反应原理及判断,题目难度中等,明确题干反应原理为解答关键,试题侧重考查学生的分析、理解能力及理解推理能力.

练习册系列答案
相关题目
7. (普)实验探究:为了研究同周期元素性质递变规律,某同学自己设计了一套实验方案,并动手记录实验步骤和现象如下:(表中的“实验步骤”与“实验现象”前后不一定是对应关系)
(普)实验探究:为了研究同周期元素性质递变规律,某同学自己设计了一套实验方案,并动手记录实验步骤和现象如下:(表中的“实验步骤”与“实验现象”前后不一定是对应关系)
请你帮助该同学整理并完成实验报告:
(1)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、AlCl3溶液、NaOH溶液、酚酞溶液等,实验所用到的玻璃仪器:①胶头滴管、试管、烧杯、酒精灯以及玻璃片等.
(2)实验内容:(填写与实验步骤对应的实验现象的编号)
(3)此实验的结论:钠、镁、铝的金属性强弱顺序为Na>Mg>Al.
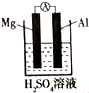
(4)该同学利用原电池原理也得出镁铝金属性的比较,他设计的原电池装置如图所示,其中正极发生的电极反应为:2H++2e-=H2↑.
 (普)实验探究:为了研究同周期元素性质递变规律,某同学自己设计了一套实验方案,并动手记录实验步骤和现象如下:(表中的“实验步骤”与“实验现象”前后不一定是对应关系)
(普)实验探究:为了研究同周期元素性质递变规律,某同学自己设计了一套实验方案,并动手记录实验步骤和现象如下:(表中的“实验步骤”与“实验现象”前后不一定是对应关系) | 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②在盛有冷水的烧杯中滴入几滴酚酞溶液,再将一小块金属钠放入其中 | B.有气体产生,溶液变成浅红色 |
| ③将镁条投入稀盐酸中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将铝条投入稀盐酸中 | D.不十分剧烈,产生无色气体 |
| ⑤向AlCl3溶液中滴加NaOH溶液至过量 | E.生成白色胶装沉淀,继而沉淀消失 |
(1)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、AlCl3溶液、NaOH溶液、酚酞溶液等,实验所用到的玻璃仪器:①胶头滴管、试管、烧杯、酒精灯以及玻璃片等.
(2)实验内容:(填写与实验步骤对应的实验现象的编号)
| 实验内容 | ① | ② | ③ | ④ | ⑤ |
| 实验现象(填A-E) | B |
(4)该同学利用原电池原理也得出镁铝金属性的比较,他设计的原电池装置如图所示,其中正极发生的电极反应为:2H++2e-=H2↑.
2.下列反应的离子方程式正确的是( )
| A. | 氧化铝和氢氧化钠溶液反应:Al2O3+2OH-=2AlO2-+H2O | |
| B. | 硫酸溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ | |
| C. | 碳酸钙跟盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| D. | 氯化铝中加入过量的氢氧化钠:Al3++3OH-═Al(OH)3↓ |
12.下列说法中正确的是( )
| A. | 近期媒体报道的某白酒中添加的塑化剂是对人体健康无害的物质 | |
| B. | 尽量使用含12C的产品,减少使用含13C或14C的产品符合“低碳经济”宗旨 | |
| C. | 大量二氧化碳气体的排放是形成酸雨的主要原因 | |
| D. | 使用太阳能、风能、潮汐能等能源能减少PM2.5的污染 |
19.氢氧燃料电池已用于航天飞机.以20%NaOH溶液为电解质溶液的这种电池在使用时的电极反应如下:
2H2+4OH--4e-=4H2O O2+2H2O+4e-=4OH-据此判断,下列说法中正确的是( )
2H2+4OH--4e-=4H2O O2+2H2O+4e-=4OH-据此判断,下列说法中正确的是( )
| A. | H2在正极发生氧化反应 | |
| B. | 燃料电池属二次电池 | |
| C. | 燃料电池的能量转化率常达100% | |
| D. | 供电时产生无污染的水,属于环境友好电池 |
17.下列说法不正确的是( )
| A. | 晶体硅是将太阳能转化为电能的常用材料 | |
| B. | 用加热的方法杀死H7N9禽流感病毒是采用了蛋白质变性原理 | |
| C. | “克隆羊”的关键技术之一是找到一些激活普通细胞的酶,并将它浸泡在酒精中保存 | |
| D. | 钠钾合金在常温下呈液态,可用于快中子反应堆作热交换剂 |
 .
.