题目内容
20.能正确表示下列反应的离子方程式是( )| A. | 氢氧化钡溶液与过量稀硫酸反应:OH-+Ba2++SO42-+H+=BaSO4↓+H2O | |
| B. | 碳酸氢钙与过量的NaOH 溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- | |
| C. | 氯化铝溶液与过量的氨水反应:Al3++4OH-=AlO2-+2H2O | |
| D. | 稀硝酸与过量的铁屑反应:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O |
分析 A.不符合离子的配比;
B.碳酸氢钙完全反应,反应生成碳酸钙、碳酸钠、水;
C.一水合氨在离子反应中保留化学式,反应生成氢氧化铝和氯化铵;
D.与过量的铁屑反应,生成硝酸亚铁.
解答 解:A.氢氧化钡溶液与过量稀硫酸反应的离子反应为2OH-+Ba2++SO42-+2H+=BaSO4↓+2H2O,故A错误;
B.碳酸氢钙与过量的NaOH 溶液反应的离子反应为Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-,故B正确;
C.氯化铝溶液与过量的氨水反应的离子反应为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.稀硝酸与过量的铁屑反应的离子反应为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
10.下列叙述错误的是( )
| A. | 砹化银难溶于水,见光容易分解 | |
| B. | H20、H2S、H2Se随着相对分子质量的增大,沸点逐渐升高 | |
| C. | 因为H2C03比H2Si03酸性强,所以将C02通入N2SiC3溶液中有H2Si03沉淀生成 | |
| D. | 铝和铊同属第IIIA族元素,但氢氧化铊[Tl(OH)3]不一定呈两性 |
8.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 2.3 g钠与水反应产生氢气的分子数为0.05NA | |
| B. | 1 mol Fe与过量的稀HNO3反应,转移2NA个电子 | |
| C. | 0.1 mol/LNa2SO4溶液含有0.1NA个SO42- | |
| D. | 22.4 L氯气与足量铜充分反应,生成1 mol CuCl2 |
5.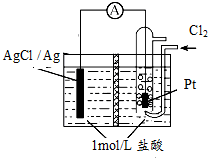 某原电池装置如图所示,中间是某种离子交换膜,电池总反应为2Ag+Cl2═2AgCl.下列说法正确的是( )
某原电池装置如图所示,中间是某种离子交换膜,电池总反应为2Ag+Cl2═2AgCl.下列说法正确的是( )
 某原电池装置如图所示,中间是某种离子交换膜,电池总反应为2Ag+Cl2═2AgCl.下列说法正确的是( )
某原电池装置如图所示,中间是某种离子交换膜,电池总反应为2Ag+Cl2═2AgCl.下列说法正确的是( )| A. | 电池放电时的负极反应为Ag-e-=Ag+ | |
| B. | 若使用阳离子交换膜,当电路中转移0.01 mol e-时,交换膜左侧溶液质量减少36.5g | |
| C. | 以Pt作电极,除了导电之外,还有催化剂的作用 | |
| D. | 用该电池给铅蓄电池充电,若有11.2L的Cl2参加电池反应,则理论上铅蓄电池的负极质量增加48g |
12. 如图装置电解一段时间,当某极析出0.32gCu时,I、Ⅱ、Ⅲ中溶液pH分别为 (溶液足量,体积均为100mL且电解前后溶液体积变化及气体的溶解忽略不计)( )
如图装置电解一段时间,当某极析出0.32gCu时,I、Ⅱ、Ⅲ中溶液pH分别为 (溶液足量,体积均为100mL且电解前后溶液体积变化及气体的溶解忽略不计)( )
 如图装置电解一段时间,当某极析出0.32gCu时,I、Ⅱ、Ⅲ中溶液pH分别为 (溶液足量,体积均为100mL且电解前后溶液体积变化及气体的溶解忽略不计)( )
如图装置电解一段时间,当某极析出0.32gCu时,I、Ⅱ、Ⅲ中溶液pH分别为 (溶液足量,体积均为100mL且电解前后溶液体积变化及气体的溶解忽略不计)( )| A. | 13、7、1 | B. | 12、7、2 | C. | 1、7、13 | D. | 7、13、1 |
9.下列说法不正确的是( )
| A. | Na2O2能与CO2反应,可用作呼吸面具的供氧剂 | |
| B. | 硅是半导体材料,可用于制备光导纤维 | |
| C. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 | |
| D. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 |
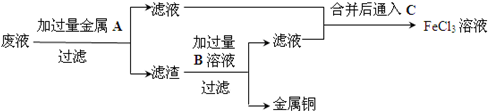

 .
.