题目内容
10.下列叙述错误的是( )| A. | 砹化银难溶于水,见光容易分解 | |
| B. | H20、H2S、H2Se随着相对分子质量的增大,沸点逐渐升高 | |
| C. | 因为H2C03比H2Si03酸性强,所以将C02通入N2SiC3溶液中有H2Si03沉淀生成 | |
| D. | 铝和铊同属第IIIA族元素,但氢氧化铊[Tl(OH)3]不一定呈两性 |
分析 A、AgAt见光易分解,结合AgCl、AgBr、AgI的性质可知,是一种不溶于水的有色固体,颜色应比AgI深;
B、水分子间存在氢键;
C、强酸制弱酸的原理分析解答;
D、铊的金属性强于铝,所以根据金属性质的变化趋势解答.
解答 解:A、AgAt见光易分解,结合AgCl、AgBr、AgI的性质可知,是一种不溶于水的有色固体,颜色应比AgI深,故A正确;
B、水分子间存在氢键,所以H20、H2S、H2Se中水的沸点最高,故B错误;
C、因为H2C03比H2Si03酸性强,根据强酸制弱酸的原理,所以所以将C02通入N2SiO3溶液中有H2Si03沉淀生成,故C正确;
D、同主族从上往下金属性增强,则铊的金属性强于铝,所以氢氧化铊[Tl(OH)3]呈碱性,故D正确;
故选B.
点评 本题考查元素周期表和元素周期律,为高频考点,A选项注意把握卤素性质的相似性、递变性为解答的关键,注意卤素元素单质之间的置换反应、非金属性强弱,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列有关说法正确的是( )
| A. | HD、H2O、NH3均为化合物 | |
| B. | CH2O2、C3H6O2、C4H8O2一定互为同系物 | |
| C. | HCOOCH3、CH3COOH、HOCH2CHO互为同分异构体 | |
| D. | SiO2、NaCl、S8、Cu均是能表示物质分子组成的分子式 |
15.短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,Y单质化学性质不活泼,而Z能形成双原子分子,是最活泼的非金属单质.根据以上叙述,下列说法中正确的是( )
| A. | 上述四种元素的原子半径大小为W<X<Y<Z | |
| B. | Z元素的最高化合价为+7价 | |
| C. | W、X、Y、Z原子的核外最外层电子数的总和为17 | |
| D. | Y元素的最高价氧化物的对应水化物能溶解所有的金属 |
2.香兰素的结构简式为: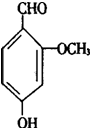 它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料,下列关于香兰素的判断不正确的是( )
它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料,下列关于香兰素的判断不正确的是( )
 它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料,下列关于香兰素的判断不正确的是( )
它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料,下列关于香兰素的判断不正确的是( )| A. | 可与银氨溶液反应 | B. | 可与氢氧化钠溶液反应 | ||
| C. | 可与浓溴水发生取代反应 | D. | 分子中所有原子都在同一平面 |
19.用玻璃棒分别蘸取下列各项中的两种浓溶液,将玻璃棒的下端相互靠近,没有白烟生成的是( )
| A. | 浓氨水和浓HNO3 | B. | 浓氨水和浓盐酸 | C. | 浓氨水和浓H2SO4 | D. | 浓氨水和浓H3PO4 |
20.能正确表示下列反应的离子方程式是( )
| A. | 氢氧化钡溶液与过量稀硫酸反应:OH-+Ba2++SO42-+H+=BaSO4↓+H2O | |
| B. | 碳酸氢钙与过量的NaOH 溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- | |
| C. | 氯化铝溶液与过量的氨水反应:Al3++4OH-=AlO2-+2H2O | |
| D. | 稀硝酸与过量的铁屑反应:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O |
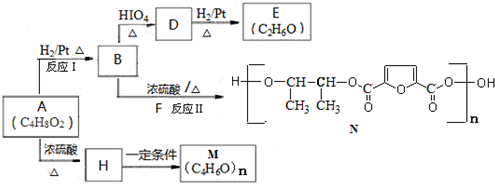
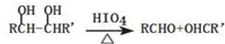
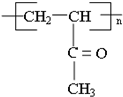 .
. .
.