题目内容
9.下列说法不正确的是( )| A. | Na2O2能与CO2反应,可用作呼吸面具的供氧剂 | |
| B. | 硅是半导体材料,可用于制备光导纤维 | |
| C. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 | |
| D. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 |
分析 A.Na2O2能与CO2、H2O反应,均生成氧气;
B.光导纤维主要成分是二氧化硅;
C.胶体遇电解质溶液发生聚沉;
D.明矾净水是利用铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质作用.
解答 解:A.Na2O2能与CO2、H2O反应,均生成氧气,所以能够做供氧剂,故A正确;
B.光导纤维主要成分是二氧化硅,不是硅,故B错误;
C.黄河中的泥沙和豆浆都是胶体,胶体遇电解质溶液发生聚沉,故C正确;
D.明矾净水是利用铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质作用,所以明矾可用作净水剂,故D正确;
故选:B.
点评 本题考查了物质的性质和用途,熟悉过氧化钠、胶体、明矾、二氧化硅的性质是解题关键,题目难度不大.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
19.用玻璃棒分别蘸取下列各项中的两种浓溶液,将玻璃棒的下端相互靠近,没有白烟生成的是( )
| A. | 浓氨水和浓HNO3 | B. | 浓氨水和浓盐酸 | C. | 浓氨水和浓H2SO4 | D. | 浓氨水和浓H3PO4 |
20.能正确表示下列反应的离子方程式是( )
| A. | 氢氧化钡溶液与过量稀硫酸反应:OH-+Ba2++SO42-+H+=BaSO4↓+H2O | |
| B. | 碳酸氢钙与过量的NaOH 溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- | |
| C. | 氯化铝溶液与过量的氨水反应:Al3++4OH-=AlO2-+2H2O | |
| D. | 稀硝酸与过量的铁屑反应:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O |
4.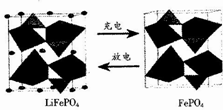 LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )
LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )
 LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )
LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )| A. | 放电时该电极为负极 | |
| B. | 充电是Li+向阳极移动 | |
| C. | 充电时该电极发生氧化反应,反应式为LiFePO4-e-=FePO4+Li+ | |
| D. | 该电池可以用磷酸溶液作电解质 |
14. (1)已知元素M是组成物质NH4Al(SO4)2的一种元素.元素M的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号I1至I4表示)如表所示:
(1)已知元素M是组成物质NH4Al(SO4)2的一种元素.元素M的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号I1至I4表示)如表所示:
元素M的名称是铝.
(2)不同元素的原子在分子内吸引电子的能力大小可用电负性来表示,下面是某些短周期元素电负性:
①通过分析电负性变化规律,确定Mg的电负性(用x表示)最小取值范围:0.9<x<1.57.
②某有机化合物结构式为 ,其中S-N中,你认为共用电子对偏向谁?氮(写原子名称)
,其中S-N中,你认为共用电子对偏向谁?氮(写原子名称)
③已知元素电负性的差值一般大于1.7时,原子间形成离子键,小于该值则原子间形成共价键,请指出下列原子之间形成的化学键是离子键还是共价键.Be和F离子键,Si和Cl共价键.
(3)工业上冶炼Z时用到的催化剂是冰晶石,制取冰晶石(Na3AlF6)的化学方程式如下:
2Al(OH)3+12HF+3A═2Na3AlF6+3CO2↑+9H2O
①反应物A的化学式为 Na2CO3,属于离子晶体
②冰晶石(Na3AlF6)是离子化合物,由两种微粒构成,冰晶石晶胞结构如图所示,“●”位于大立方体顶点和面心,“○”位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处“▽”所代表的微粒是Na+(填具体的微粒符号)
③若Na3AlF6的摩尔质量为Mg/mol,若该晶胞的边长为acm,密度为ρg/cm3,设NA表示阿伏伽德罗常数,则NA=$\frac{4M}{ρ{a}^{3}}$/mol(用M、a、ρ表示).
 (1)已知元素M是组成物质NH4Al(SO4)2的一种元素.元素M的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号I1至I4表示)如表所示:
(1)已知元素M是组成物质NH4Al(SO4)2的一种元素.元素M的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号I1至I4表示)如表所示:| I1 | I2 | I3 | I4 | |
| 电离能(kJ/mol) | 578 | 1817 | 2745 | 11578 |
(2)不同元素的原子在分子内吸引电子的能力大小可用电负性来表示,下面是某些短周期元素电负性:
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| 电负性 | 1.0 | 1.57 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.61 | 1.8 | 2.1 | 2.5 | 3.0 |
②某有机化合物结构式为
 ,其中S-N中,你认为共用电子对偏向谁?氮(写原子名称)
,其中S-N中,你认为共用电子对偏向谁?氮(写原子名称)③已知元素电负性的差值一般大于1.7时,原子间形成离子键,小于该值则原子间形成共价键,请指出下列原子之间形成的化学键是离子键还是共价键.Be和F离子键,Si和Cl共价键.
(3)工业上冶炼Z时用到的催化剂是冰晶石,制取冰晶石(Na3AlF6)的化学方程式如下:
2Al(OH)3+12HF+3A═2Na3AlF6+3CO2↑+9H2O
①反应物A的化学式为 Na2CO3,属于离子晶体
②冰晶石(Na3AlF6)是离子化合物,由两种微粒构成,冰晶石晶胞结构如图所示,“●”位于大立方体顶点和面心,“○”位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处“▽”所代表的微粒是Na+(填具体的微粒符号)
③若Na3AlF6的摩尔质量为Mg/mol,若该晶胞的边长为acm,密度为ρg/cm3,设NA表示阿伏伽德罗常数,则NA=$\frac{4M}{ρ{a}^{3}}$/mol(用M、a、ρ表示).
18.为提纯下列物质(括号中为杂质),所选除杂试剂和分离方法错误的是( )
| 选项 | 被提纯的物质(杂质) | 除杂试剂 | 分离方法 |
| A | KNO3(NaCl) | H2O | 重结晶 |
| B | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| C | 乙醇(水) | 生石灰 | 蒸馏 |
| D | 溴苯(溴) | H2O | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
19.固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3、NaNO2中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下:(注:亚硝酸:中强酸,既具有氧化性又具有还原性,不很稳定,在水溶液中易发生岐化反应.)

根据上述实验,以下说法正确的是( )

根据上述实验,以下说法正确的是( )
| A. | 溶液甲中一定含有K2SiO3、NaNO2,可能含有KAlO2、K2CO3 | |
| B. | 由于在溶液甲中加入足量稀盐酸后再加入BaCl2溶液,因此无法判断溶液中是否有K2SO3 | |
| C. | 气体A和气体D一定均为纯净物 | |
| D. | 原混合物中一定含有MnO2、Fe2O3 |