题目内容
15.近几年来关于氮污染的治理倍受关注.(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定.

①在图1所示的转化中,被还原的元素是N、O,X的化学式为Ba(NO3)2.
②SCR技术可使NOx与NH3的直接反应,实现无害转化.当NO与NO2的物质的量之比为4:1时,写出发生反应的化学方程式:8NH3+8NO+2NO2=9N2+12H2O.
(2)加入过量次氯酸钠可使废水中NH4+ 完全转化为N2,而本身被还原为NaCl.
①写出上述反应的离子方程式:2NH4++3ClO-=N2↑+3Cl-+2H++3H2O.
②若处理废水产生了0.448L N2(标准状况),则需消耗浓度为0.5mol•L-1的次氯酸钠的体积为120mL.
(3)某工业废水中含有毒性较大的CN-,可用电解法将其转变为N2,装置如图3所示.气体甲是H2(写化学式),电解池中生成N2的电极反应式为2CN-+12OH--10e-=2CO32-+N2↑+6H2O.
分析 (1)①根据化合价降低为氧化剂被还原判断;根据傅里叶红外光谱图(如图2所示)确定化合物X含硝酸根;
②根据NOx与NH3的直接反应,实现无害转化,则生成氮气和水,据此书写方程式;
(2)①根据次氯酸钠氧化废水中NH4+ 完全转化为N2,而本身被还原为NaCl结合得失电子守恒配平方程式;
②根据反应的离子方程式进行计算;
(3)由装置如图3所示,左边为阳极为CN-失电子生成氮气的反应,右边为阴极为氢离子得电子生成氢气的反应,据此分析;
解答 解:(1)①在图1所示的转化中N、O化合价降低为氧化剂被还原;由傅里叶红外光谱图(如图2所示)确定化合物X含硝酸根,再结合图一由钡离子参与,所以X为Ba(NO3)2;故答案为:N、O;Ba(NO3)2;
②因为NOx与NH3的直接反应,实现无害转化,则生成氮气和水,所以当NO与NO2的物质的量之比为4:1时,发生反应的化学方程式为8NH3+8NO+2NO2=9N2+12H2O,
故答案为:8NH3+8NO+2NO2=9N2+12H2O;
(2)①因为次氯酸钠氧化废水中NH4+ 完全转化为N2,而本身被还原为NaCl,根据得失电子守恒,离子方程式为2NH4++3ClO-=N2↑+3Cl-+2H++3H2O,
故答案为:2NH4++3ClO-=N2↑+3Cl-+2H++3H2O;
②由2NH4++3ClO-=N2↑+3Cl-+2H++3H2O得,处理废水产生了0.448L即$\frac{0.448L}{22.4L/mol}$=0.02mol N2(标准状况),则需消耗浓度为0.5mol•L-1的次氯酸钠的体积为$\frac{0.02×3}{0.5}$×1000ml=120ml,故答案为:120;
(3)由装置如图3所示,左边为阳极为CN-失电子生成氮气的反应,又溶液成碱性,所以反应式为:2CN-+12OH--10e-=2CO32-+N2↑+6H2O;右边为阴极为氢离子得电子生成氢气的反应,所以甲为氢气,
故答案为:H2;2CN-+12OH--10e-=2CO32-+N2↑+6H2O.
点评 本题重点考查了氧化还原反应以及电解池的原理,从深层次的理解氧化还原反应的本质是解决本题的关键,难度不大,注意化合价降低为氧化剂被还原,化合价升高为还原剂被氧化;

| 硼镁矿 | 硼砂 | 硼酸 | 偏硼酸钠 |
| Mg2B2O5•H2O | Na2B4O7•10H2O | H3BO3 | NaBO2 |
(1)写出硼元素在周期表中的位置第二周期ⅢA族.
(2)工业上以硼镁矿为原料制取硼,该工艺的中间过程会发生反应:B2O3+3Mg=2B+3MgO,则每生成1mol的硼转移的电子数为3NA.
(3)工业上常用金属铝冶炼难熔金属,请写出以五氧化二矾(V2O5)和铝为原料获得金属矾的化学方程式3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al2O3.
(4)硼酸是一种一元弱酸,它与水作用时结合水电离的OH-而释放出水电离的H+,皮肤上不小心碰到氢氧化钠溶液,一般先用大量水冲洗,然后再涂上硼酸溶液,请写出硼酸与氢氧化钠反应的离子方程式H3BO3+OH-=[B(OH)4]-.
(5)硼氢化钠(NaBH4)是一种强还原剂,遇水剧烈反应产生大量气体,请写出该反应的化学方程式NaBH4+2H2O═NaBO2+4H2↑.
(6)偏硼酸钠能溶于水,其溶液显碱性(填“酸性”、“中性”或“碱性”),原因是BO2-+2H2O?H3BO3+OH-(用离子方程式表示)
| A. | 冰水 | B. | 海水 | C. | 盐水 | D. | 雨水 |
| A. | 向NaOH溶液中通入过量CO2:2OH-+CO2=CO32-+H2O | |
| B. | 电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 向H2O2溶液中加入MnO2:2H2O2+4H++MnO2=O2↑+Mn2++4H2O | |
| D. | 向KAl(SO4)2溶液中滴加Ba(OH)2溶液至SO42-沉淀完全:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| A. | 钢是用量最大,用途最广的合金 | |
| B. | 苯酚沾到皮肤上,应立即用大量的热水冲洗 | |
| C. | 利用高纯单质硅,可以制成光电池 | |
| D. | 含氯,溴的氟代烷可对臭氧层产生破坏作用 |
| A. | 海水、氯水、氨水均为混合物 | |
| B. | SiO2不能和水反应,所以它不是酸性氧化物 | |
| C. | 液氨、液态氯化氢都是非电解质 | |
| D. | 冰、干冰、冰醋酸都是电解质 |
| 选项 | 实验事实 | 结论 |
| A | 将二氧化硫通入溴水中,溴水褪色 | 二氧化硫有漂白性 |
| B | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快褪为无色 | 随溶液pH减小,“84”消毒液氧化能力增强 |
| C | 铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸反应速率 |
| D | 淀粉与稀硫酸共热,再加银氨溶液水浴加热,无银镜生成 | 淀粉没有水解 |
| A. | A | B. | B | C. | C | D. | D |
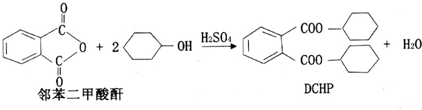
下列说法正确的是( )
| A. | DCHP的分子式为C20H28O4 | |
| B. | 上述制备DCHP的反应属于取代反应 | |
| C. | DCHP苯环上的一氯代物有4种 | |
| D. | 1 mol DCHP最多可与含4 mol NaOH的溶液反应 |