题目内容
10.下列指定反应的离子方程式正确的是( )| A. | 向NaOH溶液中通入过量CO2:2OH-+CO2=CO32-+H2O | |
| B. | 电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 向H2O2溶液中加入MnO2:2H2O2+4H++MnO2=O2↑+Mn2++4H2O | |
| D. | 向KAl(SO4)2溶液中滴加Ba(OH)2溶液至SO42-沉淀完全:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
分析 A.二氧化碳过量,反应生成碳酸氢钠;
B.氢氧化镁为沉淀,应保留化学式;
C.双氧水分解,二氧化锰做催化剂;
D.二者按照物质的量之比1:2反应SO42-沉淀完全.
解答 解:A.向NaOH溶液中通入过量CO2,离子方程式:OH-+CO2=HCO3-,故A错误;
B.电解氯化镁溶液生成氯气、氢气和氢氧化镁沉淀,离子方程式:Mg2++2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+Mg(OH)2↓,故B错误;
C.向H2O2溶液中加入MnO2,离子方程式:2H2O2$\frac{\underline{\;二氧化锰\;}}{\;}$O2↑+2H2O,故C错误;
D.向KAl(SO4)2溶液中滴加Ba(OH)2溶液至SO42-沉淀完全,反应生成硫酸钡、偏铝酸钾和水,离子方程式:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意反应物用量对反应的影响,选项AD为易错选项,题目难度中等.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
20.某混合溶液中含有NaI、NaBr、Na2SO3三种溶质,其物质的量均为l mol,向混合溶液中通入一定量的氯气.下列说法正确的是( )
| A. | 将溶液蒸干最多可以得到4 mol NaCl | |
| B. | 将溶液蒸干并灼烧,得到的固体可能是NaCl、NaBr、Na2SO4 | |
| C. | 向溶液中滴加KI淀粉溶液,溶液变蓝,则氯气一定过量 | |
| D. | 若通入氯气的体积为11.2 L(标准状况),反应的离子方程式为:2I-+Cl2=I2+2C1- |
1.科学家最近研究出一种环保、安全的制取金刚石的方法,其原理可表示为:4Na+3CO2$\frac{\underline{\;440℃高压\;}}{\;}$2Na2CO3+C,下列有关说法正确的是( )
| A. | 该反应为吸热反应 | B. | CO2中含α键又含π键 | ||
| C. | Na2CO3为离子晶体,只含离子键 | D. | 每消耗2.24LCO2生成0.4克金刚石 |
18.如图是某反应的微观示意图,下列说法不正确的是( )
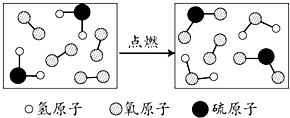

| A. | 反应物中有单质 | B. | 该反应为置换反应 | ||
| C. | 生成物的分子个数比为1:1 | D. | 化学反应前后原子的种类不变 |
2.下列叙述中正确的是( )
| A. | CuSO4溶液、稀豆浆、硅酸都能产生丁达尔效应 | |
| B. | 将NaAlO2溶液蒸干后灼烧,所得固体产物为Al2O3 | |
| C. | 标准状况下,22.4L二氯甲烷中含σ键的数目为2.408×1024 | |
| D. | 室温下,7.0g乙烯和丁烯的混合气体中含有氢原子的数目为6.02×1023 |
19.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 在反应中消耗0.1molCl2,转移的电子数一定为0.2NA | |
| B. | 15gCH3+(碳正离子)中含有的电子数为10NA | |
| C. | 标准状况下,0.5mol氦气含有的电子数为NA | |
| D. | 0.1L 2mol•L-1的(NH4)2S溶液中含有的S2-数目为0.2NA |