题目内容
20.下列叙述不正确的是( )| A. | 钢是用量最大,用途最广的合金 | |
| B. | 苯酚沾到皮肤上,应立即用大量的热水冲洗 | |
| C. | 利用高纯单质硅,可以制成光电池 | |
| D. | 含氯,溴的氟代烷可对臭氧层产生破坏作用 |
分析 A.用量最大、用途最广的合金是钢;
B.热水会烫伤皮肤;
C.高纯单质硅具有半导体性能;
D.氟氯烃会破坏臭氧层,引起臭氧层空洞.
解答 解:A.钢是用量最大、用途最广的铁合金,故A正确;
B.热水会烫伤皮肤,应用乙醇清洗,故B错误;
C.高纯单质硅具有半导体性能,所以制成的光电池可将光能直接转化为电能,故C正确;
D.氟氯烃会破坏臭氧层,引起臭氧层空洞,减少直至不使用氟氯烃可防止对大气臭氧层的破坏,故D正确.
故选B.
点评 本题考查化学与生活,侧重于危险处理和环境污染及治理,为高考常见题型和高频考点,有利于培养学生的良好科学素养,难度不大,注意相关基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列关于材料的说法,正确的是( )
| A. | 铝具有很强的抗腐蚀能力,是因为其不易与氧气发生反应 | |
| B. | 棉布,羊毛和绦纶燃烧后都生成二氧化碳和水 | |
| C. | 航天飞机上的陶瓷防护片属于新型无机非金属材料 | |
| D. | 食品保鮮膜、塑料水杯等生活用品的主要成分是聚氯乙烯 |
11.下列日常生活用品不能与水形成溶液的是( )
| A. | 食盐 | B. | 蔗糖 | C. | 白醋 | D. | 面粉 |
8.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN- | |
| B. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=106的溶液中:NH4+、K+、AlO2-、NO3- | |
| C. | 能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42-、Cl- | |
| D. | 1.0 mol•L-1的KNO3溶液中:Fe2+、H+、Cl-、I- |
5.某研究性小组探究乙酸乙酯的反应机理,相关物理性质(常温常压)及仪器如下:
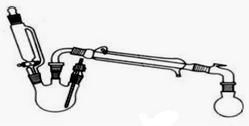
已知:当乙酸乙酯安装物质的量1:1投料时,乙酸的转化率为65%,当乙酸和乙醇按照物质的量1:10投料时,乙酸的转化率为97%(数据均在120℃下测定).
实验过程:
Ⅰ.合成反应:在三颈烧瓶中加入乙醇5mL,浓硫酸5mL,2小片碎瓷片.漏斗加入乙酸14.3 mL,乙醇20 mL.冷凝管中通入冷却水后,开始缓慢加热,控制滴加速度等于蒸馏速度,反应温度不超过120℃.
Ⅱ.分离提纯:将反应粗产物倒入分液漏斗中,依次用少量饱和的Na2CO3溶液、饱和NaCl溶液、饱和CaCl2溶液洗涤,分离后加入无水碳酸钾,静置一段时间后弃去碳酸钾.最终通过蒸馏得到纯净的乙酸乙酯.
回答下列问题:
(1)酯化反应的机理探究
A、乙醇羟基氧示踪
CH2CO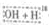 OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O
OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O
B、用醋酸烃基氧示踪

实验B发现,产物中含氧-18水占到总水量的一半,酯也一样.这个实验推翻了酯化反应为简单的取代反应的结论.请你设想酯化反应的机理先加成反应生成 后消去失水,失水有两种可能分别生成
后消去失水,失水有两种可能分别生成 .
.
(2)酯化反应是一个可逆的反应,120℃时,平衡常数K=3.45.
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)本实验用到的量取液体体积的仪器是量筒,浓硫酸与乙醇混合应怎样操作?先加入乙醇后加入硫酸,边振荡加滴加.
(5)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是保证乙醇量是乙酸量10倍以上,提高乙酸的转化率.
(6)蒸出的粗乙酸乙酯中主要有哪些杂质乙醚、乙酸、乙醇和水.用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水?减少乙酸乙酯溶解.
| 密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 | |
| 乙醇 | 0.79 | -114 | 78 | 溶 |
| 乙酸 | 1.049 | 16.2 | 117 | 溶 |
| 乙酸乙酯 | 0.902 | -84 | 76.5 | 不溶 |

已知:当乙酸乙酯安装物质的量1:1投料时,乙酸的转化率为65%,当乙酸和乙醇按照物质的量1:10投料时,乙酸的转化率为97%(数据均在120℃下测定).
实验过程:
Ⅰ.合成反应:在三颈烧瓶中加入乙醇5mL,浓硫酸5mL,2小片碎瓷片.漏斗加入乙酸14.3 mL,乙醇20 mL.冷凝管中通入冷却水后,开始缓慢加热,控制滴加速度等于蒸馏速度,反应温度不超过120℃.
Ⅱ.分离提纯:将反应粗产物倒入分液漏斗中,依次用少量饱和的Na2CO3溶液、饱和NaCl溶液、饱和CaCl2溶液洗涤,分离后加入无水碳酸钾,静置一段时间后弃去碳酸钾.最终通过蒸馏得到纯净的乙酸乙酯.
回答下列问题:
(1)酯化反应的机理探究
A、乙醇羟基氧示踪
CH2CO
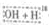 OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O
OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2OB、用醋酸烃基氧示踪

实验B发现,产物中含氧-18水占到总水量的一半,酯也一样.这个实验推翻了酯化反应为简单的取代反应的结论.请你设想酯化反应的机理先加成反应生成
 后消去失水,失水有两种可能分别生成
后消去失水,失水有两种可能分别生成 .
.(2)酯化反应是一个可逆的反应,120℃时,平衡常数K=3.45.
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)本实验用到的量取液体体积的仪器是量筒,浓硫酸与乙醇混合应怎样操作?先加入乙醇后加入硫酸,边振荡加滴加.
(5)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是保证乙醇量是乙酸量10倍以上,提高乙酸的转化率.
(6)蒸出的粗乙酸乙酯中主要有哪些杂质乙醚、乙酸、乙醇和水.用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水?减少乙酸乙酯溶解.
12.下列说法正确的是( )
| A. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| B. | 除去苯中混有的少量苯酚,加入适量NaOH溶液,振荡、静置后分液 | |
| C. | 蛋白质溶液中加入硫酸铜溶液,有沉淀产生,加水,沉淀重新溶解 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
10.下列反应I和反应II属于同一种反应类型的是( )
| 选项 | 反应Ⅰ | 反应Ⅱ |
| A | 甲烷与氯气在光照下生产一氯甲烷 | 乙烯与溴的四氯化碳溶液反应 |
| B | 乙醇催化氧化生成乙醛 | 由淀粉得到葡萄糖 |
| C | 由油脂得到甘油 | 乙烯制备聚乙烯 |
| D | 苯与浓硫酸浓硝酸反应生成硝基苯 | 乙醇和乙酸反应制备乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |


 ;反应③
;反应③ .
.