题目内容
【题目】有机化学试剂氨基氰(如图所示)常用于制备磺胺类药物,抗癌药等。下列有关氨基氰说法正确的是( )

A.属于不饱和烃B.分子中所有原子共面
C.水溶性较好D.能发生取代、加成、消去、氧化等反应
【答案】C
【解析】
氨基氰含有氨基,具有碱性,可与酸反应,含有NH键,可形成氢键,且为极性分子,可溶于水,分子中含有NC键,为δ键,可旋转,分子不一定共平面,以此解答该题。
A.氨基氰含有氨基,不属于烃,故A错误;
B.氨基氰分子中含有NC键,为δ键,可旋转,分子中所有原子不一定共平面,故B错误;
C.氨基氰含有NH键,可形成氢键,且为极性分子,可溶于水,故C正确;
D.氨基氰含有氨基,能够发生取代、氧化反应,含有碳氮三键,能够发生加成反应,但不能发生消去反应,故D错误;
故答案选C。

 阅读快车系列答案
阅读快车系列答案【题目】氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下:
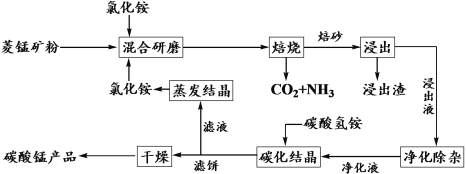
已知:①菱锰矿石主要成分是MnCO3,还含有少量Fe、Al、Ca、Mg等元素;
②相关金属离子[c(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的pH如下:
金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
回答下列问题:
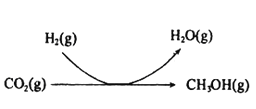
(1)“焙烧”时主要反应的化学方程式为__________________。
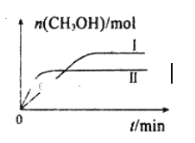
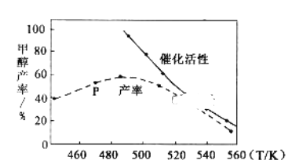
(2)分析下列图1、图2、图3,氯化铵焙烧菱镁矿的最佳条件是:_________________。

(3)浸出液“净化除杂”过程如下:首先加入MnO2将Fe2+氧化为Fe3+,反应的离子方程式为________________________;然后调节溶液pH使Fe3+、Al3+沉淀完全。
(4)碳化结晶时,发生反应的离子方程式为___________,碳化结晶过程中不能用碳酸铵溶液代替碳酸氢铵溶液可能的原因是___________________。
(5)流程中能循环利用的固态物质是____________。