题目内容
【题目】某实验小组研究溶液中AgNO3和Na2S的反应。

(1)用离子方程式解释AgNO3溶液pH<7的原因是____________________。
(2)实验小组同学认为黑色沉淀中可能含有Ag2O、Ag2S或Ag,设计实验验证。
已知:i.浓硝酸能将Ag2S转化为Ag+和SO42—(Ag2SO4可溶于硝酸);
ii. Ag2O能溶解在浓氨水中形成银氨溶液[Ag(NH2)2OH],而Ag2S和Ag均不能。
①设计并实施如下实验,证实沉淀中含有Ag2S,试剂1和试剂2分别是_________、________。

现象1中出现的现象是_______________________________。
②设计并实施如下实验,证实沉淀中不含有Ag2O,将实验操作补充完整。
实验操作 | 实验现象 | |
步骤i | 其少量银氨溶液,向其中滴加盐酸 | 出现白色沉淀 |
步骤ii | 取少量洗涤后的黑色沉淀, ____________ | 没有沉淀出现 |
写出步骤i中反应的化学方程式:_________________________。
③经检验,沉淀中不含有Ag。
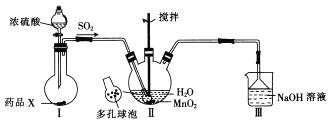
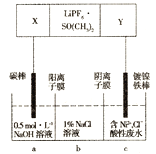
(3)实验小组同学认为AgNO3溶液具有氧化性,在一定条件下能够氧化Na2S,设计实验进行研究(实验装置如图所示),测得电压为a (a>0)。对AgNO3溶液中氧化S2—的物质进行推测:
假设1:0. 1 mol/L AgNO3溶液(pH=4)中的Ag+氧化了S2—;
假设2:0. 1 mol/L AgNO3溶液(pH=4)中的NO3—氧化了S2—
利用下图装置继续研究(已知:电压大小反映了物质氧化性与还原性强弱的差异;物质氧化性与还原性强弱的差异越大,电压越大)。

①将pH=4的0. 1 mol/L AgNO3溶液替换为_____溶液,记录电压为b(b>0)
②上述实验证实了氧化S2—的物质中一定包含了Ag+,其证据是_________实验结论:AgNO3溶液与Na2S溶液的反应类型与反应条件有关。
【答案】Ag++H2O![]() AgOH+H+ 浓硝酸 Ba(NO3)2溶液 黑色沉淀溶解,有红棕色刺激性气味的气体生成 加入浓氨水,充分振荡后过滤,向滤液中滴加足量盐酸 Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O pH=4的0.1mol/LNaNO3 a>b
AgOH+H+ 浓硝酸 Ba(NO3)2溶液 黑色沉淀溶解,有红棕色刺激性气味的气体生成 加入浓氨水,充分振荡后过滤,向滤液中滴加足量盐酸 Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O pH=4的0.1mol/LNaNO3 a>b
【解析】
硝酸银为强酸弱碱盐,其水溶液因银离子水解而呈碱性。检验沉淀为Ag2S,就要检验银离子和硫元素的存在,硫元素的存在可以通过检验硫酸根离子来间接检验。氧化银能溶于氨水得银氨溶液。设计实验时要考虑控制变量法。
(1)银离子水解使硝酸银溶液显酸性,故其pH<7,离子方程式为:Ag++H2O![]() AgOH+H+;
AgOH+H+;
(2)①检验Ag2S,先用浓硝酸检验银并且将硫离子氧化成硫酸根离子,再用钡离子检验硫酸根离子,所以试剂1是浓硝酸,试剂2是硝酸钡溶液,浓硝酸和Ag2S反应生成红棕色NO2,反应现象为:黑色沉淀溶解,有红棕色刺激性气味的气体生成;
②已知Ag2O能溶解在浓氨水中形成银氨溶液[Ag(NH3)2OH],而Ag2S和Ag均不能,参考步骤i,取少量洗涤后的黑色沉淀,加入浓氨水,充分振荡后过滤,向滤液中滴加足量盐酸,根据是否有白色沉淀生成判断沉淀中是否有Ag2O,步骤i用盐酸与银氨溶液的反应方程式为:Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O;
(3)①根据控制变量法的原理,将pH=4的0. 1 mol/L AgNO3溶液替换为pH=4的0.1mol/LNaNO3溶液;
②由题意,pH=4的0. 1 mol/L AgNO3溶液的强化性强于pH=4的0.1mol/LNaNO3溶液,氧化性越强电压差越大,则a>b;

 全能测控一本好卷系列答案
全能测控一本好卷系列答案【题目】在2 L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t ℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为______________(填“吸热”或“放热”)反应。
(2)能判断该反应是否达到化学平衡状态的依据是________。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________℃。该温度下,若向该容器中充入n(CO2)=1 mol,n(H2)=1 mol,4 min末达到平衡,CO2的转化率为_____________,H2的体积分数为_________。