题目内容
20.在一烧杯中盛有60.2gBaCO3 和BaCl2的粉末状混合物,向其中加入188.8g水使混合物中可溶物完全溶解,然后向其中逐滴加入溶质质量分数为10%的稀盐酸至146g时恰好反应完全,请根据题意回答问题:(1)在滴加盐酸过程中观察到的明显实验现象是有气体生成.
(2)当盐酸滴加至140g时,烧杯中溶液里含有溶质的是BaCl2.(写化学式)
(3)计算恰好反应完全时烧杯中所得不饱和溶液的质量.(结果精确到0.1g)
分析 (1)碳酸钡与盐酸反应生成氯化钡、二氧化碳气体和水,据此判断反应现象;
(2)加入稀盐酸至146g时恰好反应完全,据此判断当盐酸滴加至140g时溶液中溶质组成;
(3)根据化学反应BaCO3+2HCl═BaCl2+H2 O+CO2↑中HCl与CO2 的质量关系,可以求出CO2 的质量,再根据反应后溶液质量=反应前各物质的质量和-生成的气体、沉淀或杂质,即可算出恰好反应完全时烧杯中所得不饱和溶液的质量.
解答 解:(1)碳酸盐能与稀盐酸反应产生二氧化碳气体,所以在滴加盐酸过程中会观察到有气体生成,
故答案为:有气体生成;
(2)加入稀盐酸至146g时恰好反应完全,所以当盐酸滴加至140g时,BaCO3 还有剩余,但它是不溶物,所以此时溶液里含有溶质的为BaCl2,
故答案为:BaCl2;
(3)设生成二氧化碳的质量为x,
BaCO3+2HCl═BaCl2+H2O+CO2↑
73 44
146g×10% x
则:x=$\frac{146×10%×44}{73}$=8.8g,
溶液质量=60.2+188.8g+146g-8.8g=386.2g,
答:恰好反应完全时烧杯中所得不饱和溶液的质量为386.2g.
点评 本题考查了混合物反应的计算,题目难度中等,试题侧重考查学生达到分析、理解能力,明确发生反应的原理为解答关键,试题培养了学生的化学计算能力.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
10.下列分子式表示的物质一定是纯净物的是( )
| A. | C2H6O | B. | C2H4Cl2 | C. | CH4O | D. |  |
11.分子式为C8H8O2,分子结构中含有苯环且能够发生水解反应的有机物有(不考虑立体异构)( )
| A. | 3种 | B. | 5种 | C. | 6种 | D. | 7 种 |
8.下列对相应微粒的描述中,不正确的是( )
| A. | 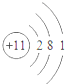 易形成阳离子 | B. | 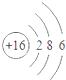 易得电子 | C. |  为稳定结构 | D. | 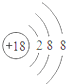 稀有气体的原子 |
12.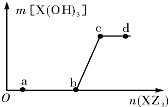 向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
 向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | d点对应的溶液中:K+、NH4+、CO32-、I- | |
| B. | c点对应的溶液中:Ag+、Ca2+、NO3-、Na+ | |
| C. | b点对应的溶液中:Na+、S2-、SO42-、Cl- | |
| D. | a点对应的溶液中:Na+、K+、SO42-、HCO3- |
11.有机物A的分子式为C6H12O3,一定条件下,A与碳酸氢钠、钠均能产生气体,且生成的气体体积比(同温同压)为1:1,则A的结构最多有( )
| A. | 33种 | B. | 31种 | C. | 28种 | D. | 19种 |