题目内容
11.有机物A的分子式为C6H12O3,一定条件下,A与碳酸氢钠、钠均能产生气体,且生成的气体体积比(同温同压)为1:1,则A的结构最多有( )| A. | 33种 | B. | 31种 | C. | 28种 | D. | 19种 |
分析 有机物分子式为C6H12O3,等量的有机物与足量的NaHCO3溶液、Na反应时产生的气体在相同条件下的体积比为1:1,说明有机物分子中含有1个-COOH、1个-OH,该有机物可以看作C5H12中2个H原子,分别被-COOH、-OH代替,结合C5H12的同分异构体判断.
解答 解:有机物分子式为C6H12O3,等量的有机物与足量的NaHCO3溶液、Na反应时产生的气体在相同条件下的体积比为1:1,说明有机物分子中含有1个-COOH、1个-OH,该有机物可以看作,C5H12中2个H原子,分别被-COOH、-OH代替,
若C5H12为正戊烷:CH3CH2CH2CH2CH3,2个H原子分别被-COOH、-OH代替,
羧基在1号碳上,此时剩余等效H为5种;
羧基连在2号碳上,剩余等效为5种;
羧基连在3号碳上,剩余等效H有3种;
若C5H12为异戊烷,羧基位于1号碳上,剩余等效H有5种;
羧基连在2号碳上,剩余等效H有3种;
羧基连在3号碳上,剩余等效H有4种;
羧基连在4号碳上,剩余等效H有4种;
若C5H12为新戊烷,羧基连在1号碳上,剩余等效H有2种,总共有31种,故选B.
点评 本题主要考查同分异构体的书写,判断有机物含有的官能团是关键,注意取代中利用定一移二进行判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是( )
| A. | 吸氢材料镧镍合金 | B. | 半导体材料砷化镓 | ||
| C. | 高温结构陶瓷材料氮化硅 | D. | 透明陶瓷材料硒化锌 |
3.X、Y、Z为短周期元素,X的单质与水在常温条件下就能剧烈反应生成一种还原性气体,Y的最高价氧化物对应的水化物是一种酸性最强的酸;Z与Y同周期且只能形成ZY3;X、Z的简单离子核外电子排布相同.下列有关叙述正确的是( )
| A. | 离子半径:X>Y>Z | B. | 最外层电子数:Y>Z>X | ||
| C. | 原子序数:Z>Y>X | D. | 单质熔点:X>Z>Y |
20.逻辑推理是化学学习中常用的一种思维方法,以下四个推理中正确的是( )
| A. | 有机物一定含有碳元素,所以含碳元素的化合物一定是有机物 | |
| B. | 置换反应中有单质生成,所以有单质生成的反应一定属于置换反应 | |
| C. | 含碳元素的物质在O2中充分燃烧会生成CO2,所以在O2中燃烧能生成CO2的物质一定含碳元素 | |
| D. | 盐的组成中含有金属阳离子与酸根离子,所以盐中一定不含氢元素 |
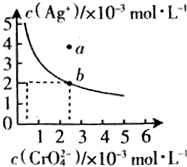 水中的沉淀溶解平衡曲线如图所示. 该温度下.下列说法正确的是AD.
水中的沉淀溶解平衡曲线如图所示. 该温度下.下列说法正确的是AD.