题目内容
10.下列分子式表示的物质一定是纯净物的是( )| A. | C2H6O | B. | C2H4Cl2 | C. | CH4O | D. |  |
分析 纯净物是由同一种物质组成,根据分子式是否存在同分异构体进行解答.同分异构体是分子式相同,但结构不同的化合物.
解答 解:A.C2H6O可以表示乙醇,也可表示甲醚,存在同分异构体,不一定是纯净物,故A错误;
B.C2H4Cl2中2个氯原子可以连接在同一碳原子上,为1,1-二氯乙烷,每个碳原子分别连接1个氯原子,为1,2-二氯乙烷,不一定是纯净物,故B错误;
C.CH4O只有一种结构,表示甲醇,不存在同分异构体,一定是纯净物,故C正确;
D.聚丙烯中聚合度n值不同,为混合物,故D错误.
故选:C.
点评 本题以纯净物为载体考查了同分异构现象,难度不大,注意纯净物必须是由同一种物质组成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.根据如表提供的信息,下列判断错误的是( )
| 第一周期 | 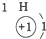 | ||
| 第二周期 | 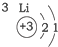 |  | 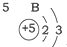 |
| 第三周期 | 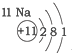 | 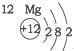 | 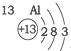 |
| A. | 元素所在的周期数等于其原子的电子层数 | |
| B. | 原子序数与元素原子核电荷数在数值上相同 | |
| C. | 第二、三周期元素的原子从左至右最外层电子数逐渐增多 | |
| D. | 金属元素的原子,其最外层电子数一般少于4个,在化学反应中易得到电子,趋向达到相对稳定结构 |
18.下列给出14种元素的电负性:
请运用元素周期律知识完成下列各题.
(1)同一周期中,从左到右,元素的电负性逐渐增大;同一主族中,从上到下,元素的电负性逐渐减小.所以,元素的电负性随原子序数的递增呈周期性变化.
(2)短周期元素中,由电负性最大的元素与电负性最小的元素形成的化合物的化学式为NaF,用电子式表示该化合物的形成过程: .
.
(3)表中符合“对角线规则”的元素有Li和Na、Be和Mg、B和Al,它们的性质分别有一定的相似性,其原因是处对角线上,写出Be(OH)2与强酸及强碱反应的离子方程式:Be(OH)2+2OH-=BeO22-+2H2O;.
(4)一般认为,两成键元素间电负性差值大于1.7时形成离子键,两成键元素间电负性差值小于1.7时,形成共价键.判断Mg3N2、SO2、AlCl3、CS2、MgO是离子化合物还是共价化合物.
离子化合物Mg3N2、MgO、共价化合物SO2、AlCl3、CS2.
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
(1)同一周期中,从左到右,元素的电负性逐渐增大;同一主族中,从上到下,元素的电负性逐渐减小.所以,元素的电负性随原子序数的递增呈周期性变化.
(2)短周期元素中,由电负性最大的元素与电负性最小的元素形成的化合物的化学式为NaF,用电子式表示该化合物的形成过程:
 .
.(3)表中符合“对角线规则”的元素有Li和Na、Be和Mg、B和Al,它们的性质分别有一定的相似性,其原因是处对角线上,写出Be(OH)2与强酸及强碱反应的离子方程式:Be(OH)2+2OH-=BeO22-+2H2O;.
(4)一般认为,两成键元素间电负性差值大于1.7时形成离子键,两成键元素间电负性差值小于1.7时,形成共价键.判断Mg3N2、SO2、AlCl3、CS2、MgO是离子化合物还是共价化合物.
离子化合物Mg3N2、MgO、共价化合物SO2、AlCl3、CS2.
5.下列说法中,正确的是( )
| A. | 离子化合物中一定不含共价键,共价化合物中一定不含离子键 | |
| B. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| C. | 碳原子之间可形成碳碳单键、碳碳双键或碳碳叁键 | |
| D. | 分子间作用力越大,分子的热稳定性就越大 |
15.某烃1mol最多能和2mol HCl加成,生成氯代烃,此氯代烃l mol能和6mol Cl2发生取代反应,生成物中只有碳氯两种元素,此烃为( )
| A. | C2H2 | B. | C2H4 | C. | C3H4 | D. | C4H6 |
2.下列说法正确的是( )
| A. | 只有共价键形成的分子一定是共价化合物 | |
| B. | 含有金属阳离子的晶体一定是离子晶体 | |
| C. | 元素的非金属性越强,其单质的活泼性一定越强 | |
| D. | 分子晶体中一定存在分子间作用力,不一定存在共价键 |
19.化学已渗透到人类生活的各个方面.下列说法正确的是( )
| A. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| B. | 严禁在写作业时将铅笔放入口中啃咬,否则会引起铅中毒 | |
| C. | 工业冶炼铝时电解Al2O3并加入冰晶石(Na3AlF6),是为了降低Al2O3的熔融温度 | |
| D. | 洗衣粉中添加三聚磷酸钠,增强去污的效果 |