题目内容
18.(1)氨是氮循环中的重要物质,氨的合成是目前普遍使用的人工固氮方法.(1)已知:H-H键能为436KJ•mol-1,N≡N键能为945KJ•mol-1,N-H键能为391KJ•mol-1.写出合成氨反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-93 KJ•mol-1
(2)可逆反应N2+3H2?2NH3在恒容密闭容器中进行,达到平衡状态的标志是②⑤
①单位时间内生成n mo1N2的同时生成3n mol H2
②单位时间内1个N≡N键断裂的同时,有6个N-H键断裂
③容器中N2、H2、NH3的物质的量为1:3:2
④常温下,混合气体的密度不再改变的状态
⑤常温下,混合气体的平均相对分子质量不再改变的状态
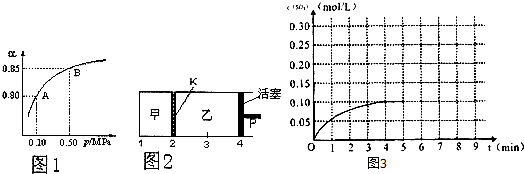
(3)恒温下,往一个2L的密闭容器中充入2.6mol H2和1mol N2,反应过程中对NH3的浓度进行检测,得到的数据如下表所:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| C(NH3)/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
(4)氨是氮肥工业的重要原料.某化肥厂以天然石膏矿(主要成分CaSO4)为原料生产铵态氮肥(NH4)2SO4,(已知Ksp(CaSO4)=7.10×10-5 Ksp(CaCO3)=4.96×10-9)其工艺流程如下:

请写出制备(NH4)2SO4的反应方程式:CaSO4+(NH4)2CO3=(NH4)2SO4+CaCO3↓;并利用有关数据简述上述反应能发生的原因因为Ksp(CaSO4)=7.10×10-5>Ksp(CaCO3)=4.96×10-9.
分析 (1)反应热=反应物总键能-生成物总键能,注明物质的聚集状态与反应热书写热化学方程式;
(2)可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不变化说明到达平衡;
(3)根据v=$\frac{△c}{△t}$计算v(NH3),再利用速率之比等于化学计量数之比计算v(N2);
恒温下,往一个2L的密闭容器中充入2.6mol H2和1mol N2,20min处于平衡状态,平衡时NH3浓度为0.2mol/L,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol/L):0.5 1.3 0
变化量(mol/L):0.1 0.3 0.2
平衡量(mol/L):0.4 1 0.2
平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$;
计算浓度商Qc,若Qc=K,处于平衡状态,若Qc>K,反应向逆反应进行,若Qc<K,反应向正反应进行;
(4)由流程图可知,硫酸钙、氨气、二氧化碳转化为(NH4)2SO4与CaCO3,CaCO3分解生成的二氧化碳循环利用,反应利用溶解度大转化为溶解度更小沉淀转化原理.
解答 解:(1)反应发生:N2(g)+3H2(g)?2NH3(g),则△H=945KJ•mol-1+3×436KJ•mol-1-6×391KJ•mol-1=-93 KJ•mol-1,反应热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-93 KJ•mol-1,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-93 KJ•mol-1;
(2)①单位时间内生成n mo1N2的同时生成3n mol H2,均表示逆反应速率,反应始终按该比例关系进行,故①错误;
②单位时间内1个N≡N键断裂的同时,有6个N-H键断裂,而1个N≡N键断裂的同时生成6个N-H键,氨气的生成与消耗速率相等,反应到达平衡,故②正确;
③容器中N2、H2、NH3的物质的量关系与氮气、氢气起始物质的量及转化率有关,不一定为1:3:2,故③错误;
④混合气体总质量不变,容器容积不变,混合气体的密度始终不变,故④错误;
⑤混合气体总质量不变,随反应进行混合气体总物质的量进行,平均相对分子质量增大,混合气体的平均相对分子质量不再改变,说明到达平衡状态,故⑤正确,
故选:②⑤;
(3)5min内,△c(NH3)=0.08mol/L,则v(NH3)=$\frac{0.08mol/L}{5min}$=0.016mol/(L.min),速率之比等于化学计量数之比,v(N2)=$\frac{1}{2}$v(NH3)=0.008mol/(L.min);
恒温下,往一个2L的密闭容器中充入2.6mol H2和1mol N2,20min处于平衡状态,平衡时NH3浓度为0.2mol/L,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol/L):0.5 1.3 0
变化量(mol/L):0.1 0.3 0.2
平衡量(mol/L):0.4 1 0.2
平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$=$\frac{0.{2}^{2}}{0.4×{1}^{3}}$=0.1;
浓度商Qc=$\frac{(0.2+\frac{2}{2})^{2}}{(0.4+\frac{2}{2})×(1+\frac{2}{2})^{3}}$=0.13>K=0.1,反应向逆反应进行,
故答案为:0.008mol/(L.min);0.1;逆反应;
(4)由流程图可知,硫酸钙、氨气、二氧化碳转化为(NH4)2SO4与CaCO3,CaCO3分解生成的二氧化碳循环利用,制备(NH4)2SO4的反应方程式:CaSO4+(NH4)2CO3=(NH4)2SO4+CaCO3,上述反应能发生的原因:因为Ksp(CaSO4)=7.10×10-5>Ksp(CaCO3)=4.96×10-9,
故答案为:CaSO4+(NH4)2CO3=(NH4)2SO4+CaCO3↓;因为Ksp(CaSO4)=7.10×10-5>Ksp(CaCO3)=4.96×10-9.
点评 本题考查化学平衡计算、平衡状态判断、反应速率计算、平衡常数、热化学方程式书写、沉淀转化等,题目比较综合,涉及知识点比较多,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等.

| A. | 分子内共价键越强,分子越稳定,其熔、沸点也越高 | |
| B. | 共价化合物溶于水,分子内共价键一定被破坏 | |
| C. | 离子键的形成一定有电子的得与失 | |
| D. | 分子晶体中一定存在分子间作用力,不一定存在共价键 |
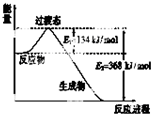 (1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1